以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如下: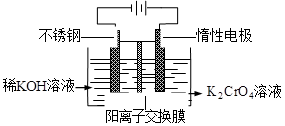
下列说法不正确的是
| A.在阴极式,发生的电极反应为:2H2O+2e-=2OH-+H2↑ |
B.在阳极室,通电后溶液逐渐由黄色变为橙色,是因为阳极区H+浓度增大,使平衡2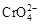 +2H+ +2H+  +H2O向右移动 +H2O向右移动 |
C.该制备过程总反应的化学方程式为:4K2CrO4+4H2O 2K2Cr2O7+4KOH+2H2↑+O2↑ 2K2Cr2O7+4KOH+2H2↑+O2↑ |
D.测定阳极液中K和Cr的含量,若K与Cr的物质的量之比为d,则此时铬酸钾的转化率为1-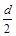 |
下列实验中,能够达到预期目的的是( )
| 编号 |
实验内容 |
实验目的 |
| A |
在Na2SO3溶液中加入HNO3酸化的Ba(NO3)2 ,产生白色沉淀 |
检验Na2SO3是否变质 |
| B |
将某气体通入品红溶液中,品红褪色 |
证明该气体是SO2 |
| C |
用洁净的玻璃棒蘸取NaOH溶液,点在湿润的pH试纸上,与标准比色卡对照 |
测定NaOH溶液的pH |
| D |
在两支试管中各加入4 mL 0.01 mol/L的KMnO4 酸性溶液,再分别加入0.1 mol/L H2C2O4 溶液2 mL、0.2 mol/L H2C2O4 溶液2 mL, 分别记录溶液褪色所需时间 |
探究相同条件下,溶液浓度对反应速率的影响 |
下列有关实验的操作、原理和现象,正确的是()
| A.减压过滤是为了加快过滤速度,得到较大颗粒的晶体 |
| B.硫酸亚铁铵晶体过滤后用无水乙醇洗涤除去其表面的杂质 |
| C.溶液、胶体各悬浊液这三种分散系的本质区别是能否透过滤纸或半透膜 |
| D.用Na2SO4的稀溶液使蛋清液发生盐析,进而分离、提纯蛋白质 |
下列除去杂质的方法正确的是( )
| A.除去CO2中混有的CO:用NaOH溶液洗气 |
| B.除去铜器表面的铜绿[Cu2(OH)2CO3]:用硝酸浸泡,再用清水冲洗 |
| C.除去KNO3晶体中少量NaCl:加水溶解,蒸发结晶 |
| D.除去Fe(OH)3固体中少量Mg(OH)2:加入足量饱和FeCl3溶液,充分搅拌后过滤 |
下列实验操作或方法中,正确的是
| A.大量氯气泄漏时,迅速离开现场,并尽量往低处去 |
| B.因为固体氯化钠溶解时热效应不大,所以可以在容量瓶中溶解氯化钠固体 |
| C.用加热的方法分离氯化钠和氯化铵固体 |
| D.用溶解、过滤的方法除去粗盐中的氯化钙和氯化镁等杂质 |
逻辑推理是化学学习中常用的一种思维方法,以下推理中正确的是( )
| A.单质都是由同种元素组成的,只含一种元素的物质一定是纯净物 |
| B.金属铝排在金属活动性顺序表中氢元素的前面,铝与酸反应一定放出氢气 |
| C.中和反应都有盐和水生成,有盐和水生成的反应都属于中和反应 |
| D.氧化物中都含有氧元素,含氧元素的化合物不一定是氧化物 |