3.9g 镁铝合金投入500mL 2mol·L-1 HCl中,金属全部溶解,再加入4mol·L-1 NaOH溶液,当沉淀达到最大量时,加入的NaOH溶液的体积为
| A.75mL | B.100mL | C.250 mL | D.无法计算 |
下列离子方程式书写正确的是
| A.氯化铜溶液与铁粉反应:Cu2++Fe = Fe2++Cu |
| B.稀 H2SO4与铁粉反应:2Fe+6H+ = 2Fe3++3H2↑ |
| C.氢氧化钡溶液与稀H2SO4反应:Ba2++SO42-=BaSO4↓ |
| D.碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑ |
下列各组离子在给定条件下能大量共存的是()
| A.在pH=1溶液中:NH4+、K+、Al3+、Cl- |
| B.有SO42-存在的溶液中:Na+、Mg2+、Ca2+、I- |
| C.有NO3-存在的强酸性溶液中:NH4+、Ba2+、Fe2+、Br- |
| D.在c(H+) =1.0×10-13 mol·L-1的溶液中:Na+、S2-、ClO-、SO32- |
将40℃的饱和硫酸铜溶液升温至50℃,或者温度仍保持在40℃而加入少量无水硫酸铜,在这两种情况下均保持不变的是
| A.硫酸铜的溶解度 | B.溶液中溶质的质量分数 |
| C.溶液的质量 | D.溶液中Cu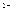 的数目 的数目 |
下列物质的分类结果全部正确的是:()
| A.苯酚——有机物纯碱——盐水——氧化物 |
| B.淀粉——混合物胆矾——纯净物漂白粉——化合物 |
| C.液氯——非电解质碳酸钙——强电解质醋酸——弱电解质 |
| D.金刚石——原子晶体食盐——离子晶体二氧化硅——分子晶体 |
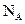 表示阿伏加德罗常数,下列判断正确的是
表示阿伏加德罗常数,下列判断正确的是
A.在18g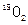 中含有 中含有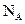 个氧原子 个氧原子 |
B.标准状况下,22.4 L水中含有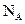 个水分子 个水分子 |
C.1 mol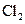 参加反应转移电子数一定为2 参加反应转移电子数一定为2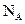 |
D.含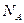 个 个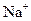 的 的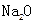 溶解于1L水中, 溶解于1L水中,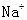 的物质的量浓度为1 mol· 的物质的量浓度为1 mol·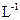 |