配制一定物质的量浓度的KOH溶液时,导致浓度偏低的原因可能是( )
| A.容量瓶中原有少量的蒸馏水 | B.移液时,不慎将液体流到瓶外 |
| C.容量瓶盛过KOH溶液,使用前未洗涤 | D.定容时俯视刻度线 |
下列有关元素周期表中的某些推断正确的是
A位于同一主族的元素的价电子数相同,则各元素的常见化合价也一定相同
B碱金属族元素同卤族元素一样,其单质的熔沸点随元素原子序数的增大而逐渐升高
C若x是ⅡB族中元素的原子序数, 那么原子序数为x+1的元素是ⅢA族
D在周期表中金属和非金属元素的分界线附近的元素是过渡元素
以下几句话中正确的有()句
①由两种元素组成的共价化合物的分子中的化学键都是极性键
②所有化学键都具有相同特征:方向性和饱和性
③分子晶体中相对分子质量越大则熔沸点一定越高
④只要是离子化合物,其熔点就比共价化合物的熔点高
⑤离子化合物形成的晶体一定是离子晶体,共价化合物形成的晶体一定是分子晶体
⑥分子晶体内可能没有共价键, 而配位化合物中一定含有配位键
⑦含有极性键的分子不一定是极性分子,含有非极性键的化合物可能是离子化合物
A 1句 B 2句 C 3句 D 4句
下列叙述不正确的是()
A金刚石晶胞(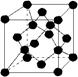 )中平均含有的碳原子数、碘晶体晶胞中平均含有的原子数均为8
)中平均含有的碳原子数、碘晶体晶胞中平均含有的原子数均为8
B二氧化硅晶体中最小环上的氧原子数、氯化铯晶体中氯离子的配位数均为6
C锌晶胞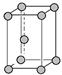 中锌原子的配位数、氯化钠晶体中距离钠离子最近且相等的钠离子数均为12
中锌原子的配位数、氯化钠晶体中距离钠离子最近且相等的钠离子数均为12
D 33g CH≡C—CH=CH—CH3中所含的π键数、12g石墨中所含的碳碳键数均为1.5mol
下列有关冰的说法中,正确的组合是()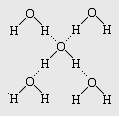
①水分子间既有氢键又有范德华力;
②每个水分子处在另外四个水分子所围成的四面体中;
③每个O原子处在四个H原子所围成的四面体中;
④晶胞与金刚石相似;
⑤与干冰的晶胞相似;
⑥每个水分子平均拥有四个氢键;
⑦冰的结构是由氢键的方向性和饱和性所决定的;
⑧冰中H和O原子之间的作用力不是σ键就是氢键
| A.除⑤⑥外 | B.除④⑦⑧外 | C.除④⑤⑥⑧外 | D.全对 |
以下有关元素性质的说法不正确的是
| A.具有下列电子排布式的原子中,①1s22s22p63s23p2②1s22s22p3③1s22s22p2 ④1s222s2p63s23p4原子半径最大的是① |
| B.具有下列价电子排布式的原子中,①3s23p1②3s23p2③3s23p3④3s23p4第一电离能最大是③ |
| C.①Na、K、Rb②N、P、Si③Na、P、Cl,元素的电负性随原子序数增大而递增的是③ |
| D.某主族元素气态基态原子的逐级电离能分别为738、1451、7733、10540、13630、17995、21703……,当它与氯气反应时生成的阳离子是X3+ |