有关X、Y、Z、W四种金属进行如下实验:
| ① |
将X和Y用导线连接,浸入电解质溶液中,Y不易腐蚀 |
| ② |
将片状的X、W分别投入等浓度盐酸中都有气体产生,W比X反应剧烈 |
| ③ |
用惰性电极电解等物质的量浓度的Y和Z的硝酸盐混合溶液,在阴极上首先析出单质Z |
根据以上事实,下列判断或推测错误的是 ( )
A.Z的阳离子氧化性最强
B.W的还原性强于Y的还原性
C.Z放入CuSO4溶液中一定有Cu析出
D.用X、Z和稀硫酸可构成原电池,且X做负极
下列说法正确的是
| A.在100℃、101 kPa条件下,1 mol液态水汽化时需要吸收40.69 kJ的热量,则H2O(g)=H2O(l)的ΔH=+40.69 kJ·mol-1 |
| B.已知CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-802.33 kJ·mol-1,则CH4的燃烧热为802.33 kJ |
| C.稀硫酸与0.1 mol·L-1NaOH溶液反应的热化学方程式为:H+(aq)+OH-(aq)=H2O(l)△ H =-57.3 kJ·mol-1 |
| D.已知S(g)+O2(g)=SO2(s) ΔH1,S(g)+O2(g)===SO2(g) ΔH2,则ΔH2<ΔH1 |
将常温下为气态的饱和链烃(碳原子数≤4)两两混合,若37g混合物与氧气完全反应,生成CO2,消耗氧气4.25mol.则此混合物的可能组合的方式最多有
| A.3种 | B.4种 | C.5种 | D.6种 |
分子式为C5H10Cl2的有机分子中,所含有的甲基数不可能为
| A.1个 | B.2个 | C.3个 | D.4个 |
下列条件下的反应,放出 最快的是
最快的是
| 金属(粉末状)/mol |
酸的浓度和体积(mL) |
反应温度 |
|||
| A |
Mg |
0.1 |
 |
10 |
20℃ |
| B |
Al |
0.1 |
 |
10 |
20℃ |
| C |
Zn |
0.1 |
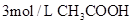 |
10 |
20℃ |
| D |
Fe |
0.1 |
 |
10 |
20℃ |
类推的思维方法在化学学习与研究中经常用到,但有时会产生错误的结论。因此,推出的结论最终要经过实践的检验才能决定其是否正确。以下几种类推结论中,正确的是
| A.第二周期元素氢化物的稳定性顺序是:HF>H2O>NH3;则第三周期元素氢化物的稳定性顺序也是:HCl>H2S>PH3 |
| B.IVA族元素氢化物沸点顺序是:GeH4>SiH4>CH4;则VA族元素氢化物沸点顺序也是:AsH3>PH3>NH3 |
| C.Fe3O4可以写成FeO·Fe2O3;Pb3O4也可以写成PbO·Pb2O3 |
| D.NaHSO4与NaHSO3溶于水显酸性,由所有酸式盐溶于水显酸性 |