正电子、负质子等都是反粒子,他们跟通常说的电子和质子相比较,质量相等,但电性相反。科学家设想,在宇宙中可能存在完全由反粒子构成的物质——反物质。物质与反物质相遇会产生“湮灭”现象,释放出巨大的能量,在能源研究领域中前景十分可观。
根据以上信息,甲、乙、丙、丁四位学生做出相应的预测:
甲:氧原子呈电中性,反氧原子带电。
乙:氧原子和反氧原子的相对原子质量都是16。
丙:氧气能供给呼吸,反氧气不能供给呼吸。
丁:氧气能支持燃烧,反氧气不能支持燃烧。
你认为:上述四位学生的预测中,一定正确的是_________,一定错误的是_________,可能正确的是____________,假设存在反氧气,请对可能正确的结论设计实验验证,方法是__________________________________________________________。
爱护水资源,落实长江大保护。
(1)树立保护水体意识。下列做法正确的有 ;
A.节约用水 B.工业用水重复利用 C.洗衣污水集中处理
(2)掌握水的净化方法。日常生活中,我们常使用活性炭制作净水器滤芯,是利用活性炭的 性,为降低水的硬度,我们常选择的方法是 ;
(3)学习净水材料制备。高铁酸钾(K2FeO4)是一种新型非氯高效水处理消毒剂,主要用于饮用水处理,制备高铁酸钾的一种模拟流程如图(部分反应条件未标出):

①K2FeO4中铁元素的化合价为 ;
②反应A、B、C、D中属于复分解反应的是 ;
③反应A的化学方程式是 。
金属的用途与性质密切相关。

|
铜 |
铝 |
|
|
密度/(g•cm﹣3) |
8.92 |
2.70 |
|
地壳中含量(质量分数/%) |
0.007 |
7.73 |
|
导电性(以银的导电性为100做标准) |
|
|
图2
(1)图1所示赤铁矿的主要成分是 (填化学式);
(2)家用电线常用铜制,但在高压远距离输电中,常用铝代替铜,请根据图2的信息分析,其原因是 ;
(3)在空气中,铝具有很好的抗腐蚀性,其原因用化学方程式表示为 ;
(4)为探究铁、铜的金属活动性,分别将铁丝、铜丝插入稀硫酸中(图3所示),说明铁比铜的金属活动性更强的实验现象是 ,反应的化学方程式是 。
(5)将一定量铝、铜粉末混合物加入硝酸银溶液中,充分反应后过滤,滤液为蓝色。则滤渣中一定含有 (填化学式,下同),滤液中溶质的组成可能是 。
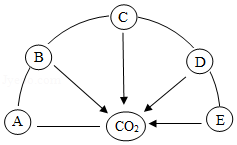
构建知识网络是一种重要的学习方法。如图是初中化学常见的单质、氧化物、酸、碱、盐五种不同类别的物质与CO2的知识网络图,“一”表示相连的两种物质能发生化学反应,“→”表示一种物质一步转化成另一种物质(部分反应条件未标出)。
请回答:
(1)A的化学式是 ,E的化学式是 ;
(2)C﹣D的化学方程式是 。
下列是实验室常用仪器,据图回答问题:

(1)认识仪器:仪器A的名称是 ;
(2)量取液体:量取5mL水,需要选择的仪器是 (填字母序号,下同);
(3)制取气体:实验室用高锰酸钾制取氧气的化学方程式是 ,用该原理制取氧气时,除上述仪器外,还缺少一种仪器的名称是 ,用向上排空气法收集氧气时,检验氧气是否收集满的方法是 。
(4)分离物质:实验室用过氧化氢溶液和二氧化锰制取氧气的化学方程式是 ,充分反应后,分离剩余的物质需进行过滤,过滤需选择的仪器是 。
下表是通过实验测得两种固体物质在不同温度时的溶解度,如图是市售果味型汽水配料表。请据图回答问题:
|
温度/℃ |
0 |
20 |
40 |
60 |
80 |
|
|
溶解度/g |
氯化钠 |
35.7 |
36.0 |
36.6 |
37.3 |
38.4 |
|
氯化钾 |
27.6 |
34.0 |
40.0 |
45.5 |
51.1 |
|
(1)20℃时,氯化钠的溶解度是 g。
(2)40℃时,将50g氯化钾放入100g水中,充分搅拌,所得溶液的质量为 g;
(3)60℃时,将45g氯化钠和45g氯化钾分别放入100g水中充分搅拌,所得氯化钠溶液溶质的质量分数 氯化钾溶液溶质的质量分数(填“<”或“>”或“=”);
(4)打开如图所示果味型汽水瓶盖时,观察到汽水中有大量气泡产生,结合配料成分可知,此时汽水是 的饱和溶液(填配料表中的具体物质)。
