在反应Fe2O3 + 3CO ="==" 2Fe + 3CO2中, 是氧化剂; 元素被氧化, 元素被还原;四种物质中, 的还原性最强;在反应中每消耗1molCO就生成 g还原产物, g氧化产物。
2010年5月15日,CCTV对“南澳一号”沉船的考古进行了两个小时的现场直播,从沉船中发现了大量宋代精美瓷器,体现了灿烂的中华文明。
青花瓷胎体的原料——高岭土[Al2Si2O5(OH)x],可掺进瓷石制胎,青花瓷釉料的成分主要是钾长石(KAlSi3O8),在1300℃左右一次烧成的釉可形成精美的青花瓷。
(1)下列说法正确的是________(填序号)。
A.高岭土分子中x=2
B.钾长石能完全溶解在盐酸中形成澄清的溶液
C.烧制青花瓷过程中发生了复杂的物理变化和化学变化
D.青花瓷、玻璃、水泥都属于硅酸盐产品
(2)在“南澳一号”考古直播过程中,需用高纯度SiO2制造的光纤。如图是用海边的石英砂(含氯化钠、氧化铝等杂质)制备二氧化硅粗产品的工艺流程: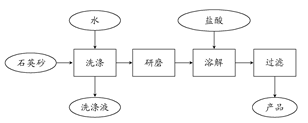
①洗涤石英砂的目的是___________________________________。
②二氧化硅与氢氧化钠溶液反应的离子方程式是______________________
③在以上流程中,要将洗净的石英砂研磨成粉末,目的是_____________。
④工业上常用纯净石英砂与C在高温下发生反应制造粗硅,粗硅中含有SiC,其中Si和SiC的物质的量之比为1:1。下列说法正确的是________(填序号)。
A.SiC性质稳定,能用于制造抗高温水泥
B.制造粗硅时的反应为:2SiO2+5C Si+SiC+4CO↑
Si+SiC+4CO↑
C.在以上流程中,将盐酸改为NaOH溶液,也可达到目的
D.纯净的SiO2只能用于制造光导纤维
铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐均为重要化合物。
(1)要确定铁的某氯化物FeClx的化学式,可用离子交换和滴定的方法。实验中称取0.54 g的FeClx样品,溶解后先进行阳离子交换预处理,再通过含有饱和OH-的阴离子交换柱,使Cl-和OH-发生交换。交换完成后,流出溶液的OH-用0.40 mol·L-1的盐酸滴定,滴至终点时消耗盐酸25.0 mL。计算该样品中氯的物质的量,并求出FeClx中x值:______________________________________ (列出计算过程);
(2)现有一含有FeCl2和FeCl3的混合物样品,采用上述方法测得n(Fe):n(Cl)=1:2.1,则该样品中FeCl3的物质的量分数为________。在实验室中,FeCl2可用铁粉和________反应制备,FeCl3可用铁粉和________反应制备;
(3)FeCl3与氢碘酸反应时可生成棕色物质,该反应的离子方程式为________________;
(4)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为_____________________________。与MnO2-Zn电池类似,K2FeO4-Zn也可以组成碱性电池,K2FeO4在电池中作为正极材料,其电极反应式为______________________,该电池总反应的离子方程式为_______________。
孔雀石的主要成分为Cu2(OH)2CO3。某校化学兴趣小组的同学设计从孔雀石中冶炼铜的方案如下: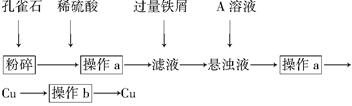
回答下列问题:
(1)在粉碎后的孔雀石中加入稀硫酸,观察到的现象是_______________。
反应的离子方程式是___________________________________________。
(2)操作a中用到的玻璃仪器是____________________________________。
(3)A的化学式为________,在悬浊液中加入A的目的是______________。
(4)操作b包括洗涤和低温烘干,作用是__________________________。
(5)有同学认为,利用铁屑和稀硫酸,不通过上述实验方案,也能从孔雀石中冶炼铜。请你用简洁的文字说明不同方案的实验原理__________________。
铁、铝、铜等金属及其化合物在日常生活中应用广泛,请根据下列实验回答问题:
(1)生产中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后,溶液中含有的大量阳离子是________。
(2)氧化铁是重要的工业颜料,用废铁屑制备它的流程如下所示。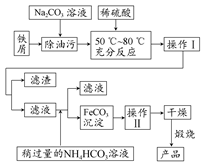
回答下列问题:
①操作Ⅰ所用的分离仪器的名称是________;操作Ⅱ的名称是________,该操作的具体方法是________。
②Na2CO3溶液可以除油污,原因是(用离子方程式表示)________。
③请写出生成FeCO3沉淀的离子方程式:________。
在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程简述如下:
Ⅰ.向废液中投入过量铁屑,充分反应后分离出固体和滤液;
Ⅱ.向滤液中加入一定量石灰水,调节溶液pH,同时鼓入足量的空气。
已知:Ksp[Fe(OH)3]=4.0×10-38
回答下列问题:
(1)FeCl3蚀刻铜箔反应的离子方程式为______________________________;
(2)过程Ⅰ加入铁屑的主要作用是________,分离得到固体的主要成分是______________,从固体中分离出铜需采用的方法是________________;
(3)过程Ⅱ中发生反应的化学方程式为______________;
(4)过程Ⅱ中调节溶液的pH为5,金属离子浓度为________。(列式计算)