25℃时,将稀氨水逐滴滴加到稀硫酸中,当溶液的pH=7时,下列关系正确的是( )
| A.c(NH4+)=c(SO42-) |
| B.c(NH4+)>c(SO42-) |
| C.c(NH4+)<c(SO42-) |
| D.c(NH4+)+c(SO42-)= c(H+)=c(NH4+) |
液态化合物AB会发生微弱的自身电离,电离方程式为AB A++B-,在不同温度下其平衡常数为K(25 ℃)=1.0×10-14,K(35 ℃)=2.1×10-14。则下列叙述正确的是()
A++B-,在不同温度下其平衡常数为K(25 ℃)=1.0×10-14,K(35 ℃)=2.1×10-14。则下列叙述正确的是()
| A.c(A+)随温度升高而降低 |
| B.在35 ℃时,c(A+)>c(B-) |
| C.AB的电离程度(25 ℃)>(35 ℃) |
| D.AB的电离是吸热过程 |
在某一体积可变的恒温密闭容器中发生如下反应:A(g)+B(g) 2C(g) ΔH<0。t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程如图所示。下列说法正确的是()
2C(g) ΔH<0。t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程如图所示。下列说法正确的是()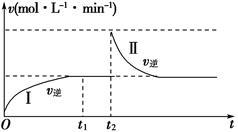
| A.0~t2时,v正>v逆 |
| B.Ⅰ、Ⅱ两过程达到平衡时,A的体积分数Ⅰ>Ⅱ |
| C.t2时刻改变的条件可以是向密闭容器中加C |
| D.Ⅰ、Ⅱ两过程达到平衡时,平衡常数Ⅰ<Ⅱ |
在密闭容器中充入一定量的NO2,发生反应2NO2(g) N2O4(g) ΔH=-57 kJ·mol-1。在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是()
N2O4(g) ΔH=-57 kJ·mol-1。在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是()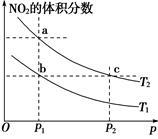
| A.a、c两点的反应速率:a>c |
| B.a、b两点NO2的转化率:a<b |
| C.a、c两点气体的颜色:a深,c浅 |
| D.由a点到b点,可以用加热的方法 |
处于平衡状态的反应2H2S(g) 2H2(g)+S2(g) ΔH>0,不改变其他条件的情况下合理的说法是()
2H2(g)+S2(g) ΔH>0,不改变其他条件的情况下合理的说法是()
| A.加入催化剂,反应路径将发生改变,ΔH也将随之改变 |
| B.升高温度,正逆反应速率都增大,H2S分解率也增大 |
| C.增大压强,平衡向逆反应方向移动,将引起体系温度降低 |
| D.若体系恒容,注入一些H2后达新平衡,H2浓度将减小 |
下列事实能说明影响化学反应速率的决定性因素是反应物本身性质的是()
| A.Cu能与浓硝酸反应,而不与浓盐酸反应 |
| B.Cu与浓硝酸反应比与稀硝酸反应快 |
| C.N2与O2在常温、常压下不反应,放电时可反应 |
| D.Cu与浓H2SO4能反应,而不与稀H2SO4反应 |