常温下,某溶液中由水电离的c(H+)=1×10-13 mol/L,该溶液可能是( )
①二氧化硫水溶液 ②氯化铵水溶液 ③硝酸钠水溶液 ④氢氧化钠水溶液
⑤硫酸氢钠 ⑥碳酸氢钠
| A.①④⑤ | B.①②⑤ | C.②③⑥ | D.④⑥ |
已知两种溶液:①0.lmol/LH2SO4溶液 ②0.2mol/LCH3COONa溶液。下列有关说法中,正确的是
| A.相同温度下,溶液中水的电离程度:溶液①>溶液② |
B.加热②,溶液中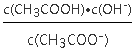 不变 不变 |
| C.等体积混合溶液①和②,所得溶液中c(CH3COO-)+2c(SO42-)=c(Na+) |
| D.25℃时,向溶液①中滴加溶液②至pH=7,溶液中c(Na+)>c(SO42-) |
随着公路上汽车流量的迅速增长,交通事故频繁发生。汽车安全气囊是在发生撞车时、产生二次碰撞前能够自动膨胀保护乘员的装置,碰撞时发生反应: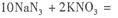
 。下列判断正确的是
。下列判断正确的是
| A.N2既是氧化剂又是还原剂 |
| B.NaN3中N元素被还原 |
| C.每生成16molN2转移30mole- |
| D.还原产物与氧化产物质量之比为l:15 |
一些烷烃的标准燃烧热如下表:
| 化合物 |
标准燃烧热(△H/KJ·mol-1) |
化合物 |
标准燃烧热(△H/KJ·mol-1) |
| 甲烷 |
-891.0 |
正丁烷 |
-2878.0 |
| 乙烷 |
-1560.8 |
异丁烷 |
-2869.6 |
| 丙烷 |
-2221.5 |
2-甲基丁烷 |
-3531.3 |
下列说法正确的是
A.热稳定性:正丁烷>异丁烷
B.正戊烷的标准燃烧热大约为:△H=一3540kJ/mol
C.乙烷燃烧的热化学方程式为:2C2H6(g)+7O2(g)→4CO2(g)+6H2O(g)+1560.8kJ/mol
D、在101kPa下,甲烷的热值是891.0kJ/g
下列解释实验事实的化学方程式正确的是
| A.FeCl3溶液中通入SO2,溶液黄色褪去:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ |
B.90℃时,测得纯水中c(H+)·c(OH-)=3.8 ×10-13:H2O(l) H+(aq)+OH-(aq)△H<0 H+(aq)+OH-(aq)△H<0 |
| C.氨水中滴入酚酞溶液.溶液变红:NH3·H2O=NH4++OH- |
| D.向苯酚钠溶液中通入CO2,溶液变浑浊:2C6H5ONa+CO2+H2O→2C6H5OH+Na2CO3 |
在密闭容器中,一定条件下进行如下反应:NO(g)+CO(g)
 N2(g)+CO2(g)△H=-373.2KJ/mol,达到平衡后,为提高NO的转化率和该反应的速率,可采取的措施是
N2(g)+CO2(g)△H=-373.2KJ/mol,达到平衡后,为提高NO的转化率和该反应的速率,可采取的措施是
| A.加催化剂同时升高温度 |
| B.加催化剂同时增大压强 |
| C.升高温度同时充入N2 |
| D.降低温度同时增大压强 |