用NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.标准状况下,22.4L己烷中共价键数目为19NA |
| B.由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA |
| C.常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3NA |
| D.1L浓度为1mol·L-1的Na2CO3溶液中含有NA个CO32- |
在一定浓度的浓硝酸中加入m克铜镁合金恰好完全溶解(假定硝酸的还原产物只有NO2),向反应后的混合溶液中滴加bmol/LNaOH溶液,当滴加到 v mL时,恰好完全反应,得到沉淀质量为n 克,则下列有关该实验的说法中正确的有( )
①沉淀中氢氧根的质量为(n-m)克 ②恰好溶解后溶液中的NO3-离子的物质的量为bv mol
③反应过程中转移的电子数为 mol ④生成NO2气体的体积为
mol ④生成NO2气体的体积为 L
L
⑤与合金反应反应的硝酸的物质的量为 mol
mol
| A.①②③④⑤ | B.①③④⑤ | C.①③⑤ | D.①②③⑤ |
关于海水综合利用问题,下列说法错误的是()
| A.从能量转换角度来看,氯碱工业中的电解饱和食盐水是一个将电能转化为化学能的过程 |
| B.在过程②中若要获得无水MgCl2不可直接蒸干灼烧 |
| C.除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸 |
| D.第③④步的目的是为了浓缩富集溴 |
下列用数轴表示的产物与量的关系不合理的是()
| A.铁与稀硝酸反应: |
 |
| B.Cl2与FeI2溶液反应后的产物: |
 |
| C.向烧碱液中通入SO2后的产物: |
 |
| 向AlCl3溶液中滴加NaOH溶液,铝元素的存在形式: |
 |
下列陈述Ⅰ、Ⅱ正确并且有因果关系的是()
| 选项 |
陈述Ⅰ |
陈述Ⅱ |
| A |
SO2和氯水有漂白性 |
两者都能使溴水褪色 |
| B |
C的还原性比Si强 |
C与SiO2反应得到硅单质 |
| C |
盐酸和氨水能溶解Al(OH)3 |
Al(OH)3是两性氢氧化物 |
| D |
CuSO4可以使蛋白质变性 |
误食铜盐使人中毒 |
某溶液中可能含有H+、NH4+ 、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示,则下列说法不正确的是()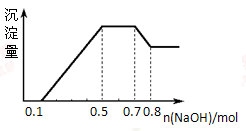
| A.溶液中的阳离子有H+、Mg2+、Al3+、NH4+ |
| B.溶液中n(NH4+ )=0.2mol |
| C.溶液中一定不含CO32-和NO3-,可能含有SO42- |
| D.n(H+):n(Al3+):n(Mg2+)=2:2:1 |