已知化合物B3N3H6(硼氮苯)与C6H6(苯)的分子结构相似,如图所示: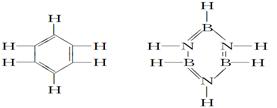
则硼氮苯的二氯取代物B3N3H4Cl2的同分异构体的数目为 ( )
| A.2 | B.3 | C.4 | D.6 |
某温度时,用惰性电极电解硝酸钠的不饱和溶液。若两极板收集到气体总体积为22.4aL时,剩余溶液恢复至原温度,析出溶质mg;若两极收集到气体总体积为33.6aL时,剩余溶液恢复至原温度,析出溶质ng。则硝酸钠在该温度时的溶解度是(气体体积均已折合为标准状况下的体积
A.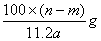 |
B. |
C.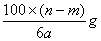 |
D.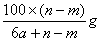 |
用惰性电极电解一定浓度的硫酸铜溶液,长时间通电后,向所得溶液中加入0.2mol Cu(OH)2,恰好恢复到电解前的浓度和pH。则电解过程中转移电子的总物质的量为
| A.0.2mol | B.0.4mol | C.0.6mol | D.0.8mol |
石油原油没有固定的沸点,加热原油使其不同沸点的组分分别汽化,再分别冷凝,可分离得到汽油、煤油和沥青等物质。据此判断,石油是
| A.混合物 | B.化合物 | C.单质 | D.纯净物 |
下列物质中,在一定条件下既能起加成反应,也能起取代反应,但不能使KMnO4酸性溶液退色的是
| A.丙烯 | B.苯 | C.甲苯 | D.丙炔 |
甲苯分子的二氯取代物的同分异构体共有
| A.4种 | B.6种 | C.8种 | D.10种 |