某有机物的结构简式为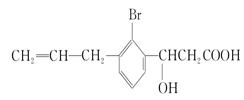 ,则此有机物可发生反应的类型有( )
,则此有机物可发生反应的类型有( )
①取代反应 ②加成反应 ③消去反应 ④水解反应 ⑤氧化反应 ⑥加聚反应
| A.①②③⑤⑥ | B.②③④⑤⑥ |
| C.①②④⑤⑥ | D.①②③④⑤⑥ |
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中只有X是短周期的金属元素,下列判断正确的是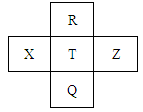
| A.X的最高价氧化物能溶于强碱 |
| B.非金属性:T<R |
| C.气态氢化物稳定性:T>Z |
| D.R与Q的原子核外电子数相差16 |
如图所示的电化学装置,下列叙述正确的是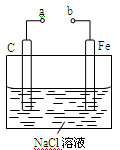
| A.a和b用导线连接,电子由碳经过导线流向铁 |
| B.a和b用导线连接,铁电极的电极反应为:Fe-3e-=Fe3+ |
| C.a、b分别连接直流电源正、负极,可以防止铁被腐蚀 |
| D.a、b分别连接直流电源负、正极,电压足够大时,Na+向铁电极移动 |
下列实验操作正确且能达到目的的是
| A.用NH4Cl溶液蒸干制备NH4Cl固体 |
| B.用重结晶法除去KNO3中混有的NaCl |
| C.用BaCl2溶液鉴别AgNO3溶液和K2SO4溶液 |
| D.用NaOH溶液和分液漏斗萃取溴水中的溴 |
常温下,有体积相同的四种溶液:①pH=3的CH3COOH溶液;②pH=3的盐酸;③pH=11的氨水;④pH=11的NaOH溶液。下列说法正确的是
| A.①和②混合溶液中:c(H+)=3.0 mol·L-1 |
| B.①和④混合溶液中:c(Na+)=c(CH3COO-)+c(CH3COOH) |
| C.②和③混合溶液中:c(Cl-)+c(H+)>c(NH4+)+c(OH-) |
| D.四种溶液稀释100倍,溶液的pH:③>④>②>① |
下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是
| 选项 |
叙述Ⅰ |
叙述Ⅱ |
| A |
Cl2有酸性 |
用Cl2可与石灰乳或烧碱反应制备含氯消毒剂 |
| B |
NaHCO3溶于水完全电离 |
NaHCO3是强电解质 |
| C |
浓H2SO4有强氧化性 |
浓H2SO4可用于干燥SO2 |
| D |
Na2S有强还原性 |
用于除去废水中的Cu2+和Hg2+ |