用NA表示阿伏加德罗常数,下列说法中正确的是( )
| A.2 L 0.1 mol·L-1 K2SO4溶液中离子所带电荷总数约为0.6 NA |
| B.标准状况下,22.4 L任意比的氢气和氯气的混合气体中含有的原子总数均为NA |
| C.1 mol Cl2变为Cl-时得到的电子数为NA |
| D.在常温常压下,18g水所含的电子数目为10NA |
下列有关实验的选项正确的是
|
.配制0.10
溶液 |
.除去 中的 |
.苯萃取碘水中的
分出水层后的操作 |
.记录滴定终点读数为12.20 |
 |
 |
 |
 |
碳酸亚乙酯是锂离子电池低温电解液的重要添加剂,其结构如下图。下列有关该物质的说法正确的是
| A. | 分子式为 |
| B. | 分子中含6个 键 |
| C. | 分子中只有极性键 |
| D. | 8.6 该物质完全燃烧得到6.72 |
某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为
、
、
,不考虑其他杂质)制取七水合硫酸亚铁(
),设计了如下流程:
下列说法不正确的是()
| A. | 溶解烧渣选用足量硫酸,试剂 选用铁粉 |
| B. | 固体1中一定含有 ,控制pH是为了使 转化为 ,进入固体2 |
| C. | 从溶液2得到 产品的过程中,须控制条件防止其氧化和分解 |
| D. | 若改变方案,在溶液1中直接加 至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到 |
40℃时,在氨-水体系中不断通入
,各种离子的变化趋势如下图所示。下列说法不正确的是()
| A. | 在 =9.0时, ( )> ( )> ( )> ( ) |
| B. | 不同pH的溶液中存在关系: ( )+ ( )=2 ( )+ ( )+ ( )+ ( ) |
| C. | 随着 的通入, 不断增大 |
| D. | 在溶液中 不断降低的过程中,有含 的中间产物生成 |
在固态金属氧化物电解池中,高温共电解 混合气体制备 和 是一种新的能源利用方式,基本原理如图所示。下列说法不正确的是()
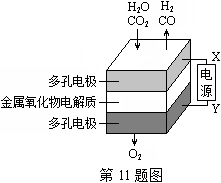
| A. | 是电源的负极 |
| B. |
阴极的反应式是:
|
| C. | 总反应可表示为: |
| D. | 阴、阳两极生成的气体的物质的量之比是1︰1 |