金刚石和石墨是碳元素的两种结构不同的单质。在100 kPa时,1 mol石墨转化为金刚石,要吸收1.895 kJ的热能。据此,试判断在100 kPa压强下,下列结论正确的是
| A.石墨比金刚石稳定 |
| B.金刚石比石墨稳定 |
| C.1 mol石墨比1 mol金刚石的总能量高 |
| D.1 mol石墨比1 mol金刚石的总能量低 |
在海水的综合利用中,海水提溴工业是一个重要组成部分,其中一种提溴的工艺是在预先浓缩并酸化的海水中,通入足量氯气,然后使生成的溴与吸收剂SO2反应转化为氢溴酸以达到富集溴元素的目的。在有关上述工艺流程的以下化学用语中,正确的是
A.用电子式表示溴化氢的形成过程为: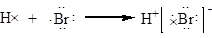 |
B.海水中Br-的电子式为: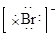 |
| C.海水中通入氯气时发生反应的离子方程式为:2NaBr+Cl2=Br2+2NaCl |
D.氯离子的结构示意图为: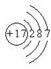 |
已知2 mol氢气完全燃烧生成水蒸气时放出能量484 kJ,且氧气中1 mol O=O键完全断裂时吸收能量496 kJ,水蒸气中1 mol H–O键形成时放出能量463 kJ,则氢气中1 mol H–H键断裂时吸收能量为
| A.920 kJ | B.557 kJ | C.436 kJ | D.188 kJ |
获得“863”计划支持的环境友好型铝碘电池已研制成功,电解质溶液为AlI3溶液,电池总反应式为2Al+3I2=2AlI3。下列说法不正确的是
| A.该电池负极的电极反应为:Al–3e-=Al3+ |
| B.电池工作时,溶液中铝离子向正极移动 |
| C.消耗相同质量金属时,用锂作负极产生电子的物质的量比用铝时多 |
| D.当导线中有3.612×1024个电子通过时,电池负极质量减少27 g |
化合物在水中能电离出具有相同电子层结构的阴阳离子,该化合物可能为
| A.H2O | B.Na2O | C.KCl | D.Na2S |