下列各组热化学方程式中,化学反应的△H前者大于后者的是
①C(s)+O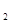 (g)==CO
(g)==CO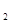 (g) △H
(g) △H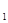 C(s)+
C(s)+ O
O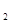 (g)==CO(g) △H
(g)==CO(g) △H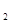
②S(s)+O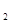 (g)==SO
(g)==SO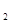 (g) △H
(g) △H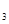 S(g)+O
S(g)+O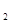 (g)==SO
(g)==SO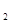 (g) △H
(g) △H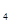
③H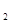 (g)+
(g)+ O
O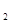 (g)==H
(g)==H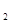 O(l) △H
O(l) △H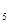 2H
2H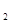 (g)+O
(g)+O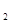 (g)==2H
(g)==2H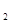 O(l) △H
O(l) △H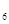
④CaCO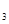 (s)==CaO(s)+CO
(s)==CaO(s)+CO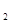 (g) △H
(g) △H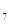 CaO(s)+H
CaO(s)+H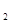 O(l)==Ca(OH)
O(l)==Ca(OH)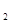 (s) △H
(s) △H
| A.①② | B.③④ | C.②③④ | D.②③ |
除去某物质里混有的少量杂质,下列做法中不正确的是(括号内的物质为杂质)
| A.KNO3溶液(AgNO3):加足量KCl溶液后过滤. |
| B.NaCl溶液(Na2CO3):加足量盐酸后加热. |
| C.KNO3固体(NaCl):溶解后加热蒸发得浓溶液,降温结晶后过滤. |
| D.NaCl溶液(BaCl2):加过量Na2CO3溶液,过滤,再加适量盐酸并加热. |
下图所示的实验操作中,正确的是()
下列实验操作正确的是()
| A.硫酸钠中含有少量碳酸钠,加入盐酸除去碳酸钠杂质 |
| B.萃取时,将酒精和碘化钾溶液放入分液漏斗中静置分层 |
| C.用分液漏斗分离互不相容的两种液体时,先放出下层液体,然后再放出上层液体 |
| D.配制一定物质的量浓度溶液定容时,用胶头滴管滴加蒸馏水至溶液凹液面最低点与刻度线相切 |
实验室进行过滤和蒸发操作时,都要用到的仪器是()
| A.烧杯 | B.蒸发皿 | C.玻璃棒 | D.酒精灯 |
用NA表示阿伏加德罗常数,64gSO2含有氧原子数为()
| A.1NA | B.2NA | C.3NA | D.4NA |