反应N2O4(g) 2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化如图示曲线。下列说法正确的是
2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化如图示曲线。下列说法正确的是
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深、C浅
C.由状态B到状态A,可以用加热的方法
D.A、C两点气体的平均相对分子质量:A>C
下列有关图像的分析正确的是()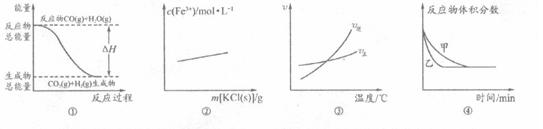
A.图①表示反应“CO(g)+H2O(g) CO2(g)+H2(g)”中的△H大于0 CO2(g)+H2(g)”中的△H大于0 |
B.图②可表示反应“3KSCN+FeCl3 Fe(SCN)3+3KCl”向正反应方向移动 Fe(SCN)3+3KCl”向正反应方向移动 |
C.图③表示反应“A2(g)+3Br(g) 2AB3(g)”的△H小于0 2AB3(g)”的△H小于0 |
D.图④可表示压强对反应“2A(g)+2B(g) 3C(g)+D(s)”的影响,且乙 3C(g)+D(s)”的影响,且乙 的压强大 的压强大 |
某燃料电池所用燃料为H2和空气,电解质为熔融的K2CO3。该电池的总反应为2H2+O22H2O,负极反应为H2+CO32――2e-H2O+CO2。下列说法正确的是()
| A.放电时CO32-向负极移动 |
| B.该电池正极反应式为:4OH――4e- |
| C.电池放电时,电池中CO32-数目逐渐减少 |
| D.电池放电时,电子经正极、负极、熔融的K2CO3后再回到正极,形成闭合回路 |
常温下,下列数据在比值为2:1的是()
A.0.2 mol/L的CH3COOH溶液与0.1 mol/ L的盐酸溶液中的c(H+)之比 L的盐酸溶液中的c(H+)之比 |
| B.pH=12的Ba(OH)2和pH=12的KOH溶液中溶质的物质的量之比 |
| C.Na2CO3溶液中:c(Na+)与c(CO32-)之比 |
| D.pH=7的氨水和(NH4)2SO4混合溶液中:c(NH4+)与c(SO42-)之比 |
下列说法或表示正确的是()
| A.将等质量硫蒸气和硫粉分别完全燃烧,前者放出热量多 |
B.由“C(石墨)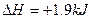 ·mol-1可知金刚石比石墨稳定 ·mol-1可知金刚石比石墨稳定 |
| C.稀的强酸和稀的强碱溶液反应的热化学方程式均为: H++OH- 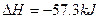 ·mol-1 ·mol-1 |
| D.在25℃、101 kPa时,1克氢气完全燃烧生成H2O放出热量142.9kJ。则: |
2H2O(1)2H2(g)+ O2(g);
O2(g);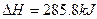 ·
· mol-1
mol-1
下列实验操作中,先后顺序正确的是()
| A.在进行中和滴定是,先固定沉定管,后润洗、装液 |
| B.测定硫酸铜晶体的结晶水含量时,先称取一定量的晶体,后放入坩埚 |
| C.为检验酸性溶液中的Cl-和SO42-,先加硝酸银溶液,滤去沉淀后加硝酸钡溶液 |
| D.实验室抽取干燥纯净的氯气时,先使氯气通过饱和食盐水,后通过浓硫酸 |