将一定量的钠铝合金置于水中,合金全部溶解,得到20 mL pH=14的溶液,然后用1mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如图所示,则下列选项正确的是( )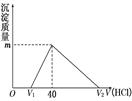
| A.原合金质量为0.92 g |
| B.标准状况下产生氢气896 mL |
| C.图中m值为1.56 g |
| D.图中V2为60 mL |
下列表述正确的是:
| A.NaHCO3溶液中:c(H+) + c(H2CO3) = c(OH-) |
| B.中和等体积、等pH相同的盐酸和CH3COOH溶液所消耗的NaOH物质的量相同 |
| C.pH=2的HA溶液与pH=12的MOH溶液以任意比混合后,所得溶液中: c(H+) + c(M+) = c(OH-) + c(A-) |
| D.在水电离出的H+浓度为1×10-12 mol/L的溶液中,K+、NO3-、I-一定能大量共存 |
下列说法正确的是
| A.淀粉和纤维素的化学式均为(C6H10O5)n,二者互为同分异构体 |
| B.从形式上看,酯化反应也属于取代反应 |
| C.油脂的相对分子质量都较大,所以属于高分子化合物 |
| D.乙烯能使酸性高锰酸钾溶液和溴水褪色,二者反应原理相同 |
下列有关沉淀溶解平衡的说法正确的是:
A.KSP(AB2)小于KSP(CD),说明AB2的溶解度小于CD的溶解度
B.在氯化银的沉淀溶解平衡体系中,加入蒸馏水,氯化银的KSP增大
C.已知25℃时,KSP(AgCl)大于KSP(AgI),若向氯化银沉淀溶解平衡体系中,加入足量碘化钾固体,则有黄色沉淀生成
D.在碳酸钙的沉淀溶解平衡体系中,加入稀盐酸,平衡不移动
下列实验设计和结论不相符的是:
| A.某无色无味气体通入澄清石灰水中,石灰水变浑浊,则该气体为CO2 |
| B.某气体能使湿润的红色石蕊试纸变蓝,则该气体水溶液显碱性 |
| C.某无色溶液中加入盐酸酸化的BaCl2溶液,产生白色沉淀,则该溶液中一定有SO42- |
| D.用可见光束照射某红褐色液体产生丁达尔现象,则该液体为胶体 |
下列各组离子,一定能大量共存的是:
| A.常温下,c(H+)/c(OH-)=1×10-12的溶液:I-、Cl-、HCO3-、Na+ |
| B.含有大量Fe3+的溶液:Na+、HCO3-、NO3-、CO32- |
| C.加入铝粉能产生氢气的溶液:NH4+、Fe2+、SO42-、Cl- |
| D.pH试纸变深红色的溶液中:NH4+、Ca2+ 、Cl-、K+ |