(10分) 某同学用如图所示装置探究SO2的性质及其有关实验.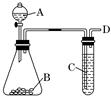
(1)实验室用亚硫酸钠固体和一定浓度的硫酸反应制备SO2气体,写出该反应的化学方程式______________________________________________________________
(2)分别将SO2气体通入下列C溶液中,请回答下列问题:
①少量SO2通入紫色石蕊试液,现象是______________,继续通入过量SO2气体,现象是________________.
②SO2通入紫色KMnO4溶液,现象是______________,其反应的离子方程式为_______________________.
③过量SO2慢慢地通入澄清石灰水中,现象___________________________________
④若C为双氧水,则通入SO2后,请大胆判断所得溶液是________(填溶质的化学式),若该同学制备的SO2气体中混有CO2气体,产生杂质的原因可能是亚硫酸钠固体中混有__________.
I.在实验室利用下列装置,可制备某些气体并验证其化学性质。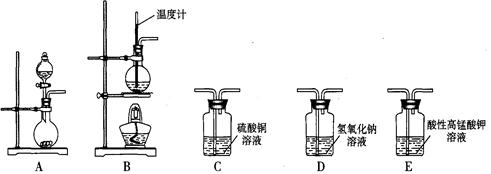
完成下列表格:
| 序号 |
气体 |
装置连接顺序(填字母) |
制备反应的化学方程式 |
| (1) |
乙烯 |
__________________ |
_________________________ |
| (2) |
乙炔 |
A→C→E |
_________________________ |
II. (1)工业上用乙烯和氯气为原料,经下列各步合成聚氯乙烯(PVC):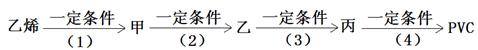
反应(2)的化学方程式是__________________________________________;
PVC的结构简式是_________________________________________________。
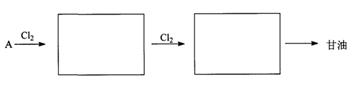
(2)石油被称为“工业血液”。A是从石油中得到的链状烃,相对分子质量为42。以A为原料,利用下述反应合成甘油,在方框内填上中间体的结构简式。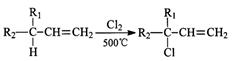
将4 g NaOH溶于_________g 水中,可使溶液中H2O与Na+的物质的量之比为20:1,此溶液中溶质的质量分数为;若测得该溶液的密度为1.1 g·cm-3,则该溶液体积为(精确到小数点后1位),溶液中c(Na+)为_________(精确到小数点后2位)。
15.6 g Na2X2含Na+ 0.4 mol,则Na2X2的摩尔质量为__________,X的相对原子质量为__________。
将4 g NaOH溶于水,配制成250 mL溶液A,A的物质的量浓度为____________;取10 mL A溶液,加水稀释至100 mL后,得到溶液B,B的物质的量浓度为_____________。
0.6 mol O2和0.4 mol臭氧(O3)的质量________(填“相等”或“不相等”,下同),它们所含的分子数__________,所含的氧原子数___________。