工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下:
下列叙述正确的是
| A.反应②的化学方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3 |
| B.反应①、过滤后所得沉淀为氢氧化铁 |
| C.图中所示转化反应都不是氧化还原反应 |
| D.试剂X可以是氢氧化钠溶液,也可以是盐酸 |
实验室中需要0.2 mol·L-1的CuSO4溶液950 mL,配制时应选用的容量瓶的规格和称取胆矾晶体(CuSO4·5H2O)的质量分别是
| A.950 mL 30.4 g | B.950 mL 47.5g |
| C.1000 mL 50.0 g | D.1000 mL 32.0g |
在下列反应中,水既不是氧化剂,也不是还原剂的是
| A.2Na+2H2O=2NaOH+H2↑ | B.Cl2+H2O HCl +HClO HCl +HClO |
| C.2F2+2H2O=4HF+O2 | D.2H2O H2↑+O2↑ H2↑+O2↑ |
不能实现下列物质间直接转化的元素是:
单质 氧化物
氧化物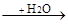 酸或碱
酸或碱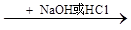 盐
盐
| A.碳 | B.钠 | C.硫 | D.铁 |
下列各物质属于电解质的是
① NaOH ②BaSO4 ③Cu ④蔗糖 ⑤CO2
| A.①② | B.①②⑤ | C.③④ | D.①③⑤ |
在物质分类中,前者包括后者的是
| A.氧化物、化合物 | B.盐、电解质 | C.溶液、 胶体 | D.分散系、溶液 |