用NA表示阿伏加德罗常数的值。下列叙述正确的是( )
| A.常温常压下的33.6L氯气与足量铝充分反应,转移电子数为3NA |
| B.由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA |
| C.由2H和18O所组成的水11克,其中所含的中子数为4NA |
| D.1 L浓度为l mol·L-1的Na2CO3溶液中含有NA个CO32- |
设NA为阿伏加德罗常数的值,下列叙述正确的是
①常温常压下,18g14CH4所含中子数目为8 NA
②1L0.1mol·L-1的氨水中有NA个NH4+
③1mol Na2O2中含有NA个阴离子
④1L1mol·L-1NaClO 溶液中含有ClO-的数目为NA
⑤78g 苯含有C=C双键的数目为3NA
⑥0.1molN2和0.3molH2在某密闭容器中充分反应,转移电子的数目为0.6NA
⑦60gSiO2晶体中含有硅氧键的数目为4NA
| A.①③⑦ | B.②③⑥ | C.②④⑥ | D.①④⑤⑦ |
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,下列结论正确的是
| W |
X |
|
| Y |
Z |
A.X、Y、Z中最简单氢化物稳定性最弱的是Z
B.Z元素氧化物对应水化物的酸性一定强于Y
C.Z元素单质在化学反应中只表现氧化性
D.X、Y、Z元素形成的单核阴离子还原性最强的是Y
莽草酸的结构简式如下图所示,可用来合成药物达菲,下列关于莽草酸的说法错误的是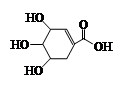
| A.分子式为C7H10O5 |
| B.分子中含有两种官能团 |
| C.既可发生加成又可发生取代反应 |
| D.能够使酸性高锰酸钾溶液和溴水褪色 |
化学与生活密切相关,下列叙述中不正确的是
| A.户外钢架桥生锈主要是电化学腐蚀所致 |
| B.导电塑料是应用于电子工业的一种新型有机高分子材料 |
| C.CO2、NO2或SO2都会导致酸雨的形成 |
| D.葡萄中的花青素在碱性环境下显蓝色,故可用苏打粉检验假红酒 |
将一定量的镁和铜组成的混合物加入到稀硝酸中,金属完全溶解(假设反应中还原产物只有NO)。向反应后的溶液中加入3 mol/L NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1 g。下列叙述不正确的是
| A.当生成的沉淀量达到最大时,消耗NaOH溶液的体积V≥100 mL |
| B.当金属全部溶解时收集到NO气体的体积一定为2.24 L |
| C.参加反应的金属的总质量3.6 g<m<9.6 g |
| D.当金属全部溶解时,参加反应的硝酸的物质的量一定是0.4 mol |