下列离子方程式正确的是( )
| A.石灰石溶于醋酸: CaCO3 + 2CH3COOH = 2CH3COO-+ Ca2+ + CO2↑+ H2O |
| B.钠与硫酸铜溶液反应: Cu2+ + 2Na = 2Na+ + Cu |
| C.铁屑溶于过量稀硝酸:3Fe + 8H+ + 2NO3-=3Fe2+ + 2NO↑+ 4H2O |
| D.FeCl2溶液中通入少量氯气:Fe2+ + Cl2= Fe3+ + 2Cl- |
下列说法正确的是
| A.31g红磷变成31g白磷要吸收能量,说明白磷比红磷更稳定 |
| B.Ba(OH)2·8H2O 与NH4Cl 的反应是放热反应 |
| C.断开1mol H2O分子中的化学键所释放的能量与形成相等质量的H2O分子中的化学键所吸收的能量相等 |
| D.铝热反应中, 2molAl和1molFe2O3的总能量比2molFe和1molAl2O3的总能量高 |
下列有关化学反应速率的说法中,正确的是
| A.100 mL 2 mol/L盐酸与锌反应时,加入适量的氯化钠溶液,生成氢气的速率不变 |
B.对于可逆反应2CO + 2NO  N2 + 2CO2,使用合适的催化剂,CO的生成速率和消耗速率都加快 N2 + 2CO2,使用合适的催化剂,CO的生成速率和消耗速率都加快 |
| C.二氧化硫的催化氧化是一个放热反应,升高温度,正反应速率减慢 |
| D.用铁片和稀硫酸反应制取氢气时,改用铁片和浓硫酸可以加快氢气的产生 |
下列有关电池的说法错误的是
| A.手机上用的锂离子电池属于二次电池 |
| B.铅蓄电池中负极为铅,电解质是硫酸 |
| C.氢氧燃料电池正极输入氢气,负极输入空气 |
| D.锌锰干电池即使不用,长久放置也会失效 |
将等质量的两份锌粉a、b分别加入过量的稀硫酸,同时向a中加少量CuSO4溶液,下图中产生H2的体积V(L)与时间t(min)的关系,其中正确的是
下列说法正确的是
| A.H2O和H2O2中的化学键类型完全相同 |
| B.N2的结构式为N—N |
| C.一个D2O分子所含的中子数为10(质量数:D-2,O-16) |
D.NaCl的电子式为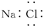 |