有一合金由X、Y、Z、W四种金属组成,若将合金放入盐酸中只有Z、Y能溶解;若将合金置于潮湿空气中,表面只出现Z的化合物;若将该合金做阳极,用X盐溶液作电解液,通电时四种金属都以离子形式进入溶液中,但在阴极上只析出X。这四种金属的活动性顺序是
| A.Y>Z>W>X | B.Z>Y>W>X |
| C.W>Z>Y>X | D.X>Y>Z>W |
在一密闭容器中通入A、B两种气体,在一定条件下发生反应2A(g)+B(g)  2C(g) ΔH<0,当反应达到平衡后,改变一个条件(x),下表中量(y)一定符合下图中曲线的是( )
2C(g) ΔH<0,当反应达到平衡后,改变一个条件(x),下表中量(y)一定符合下图中曲线的是( )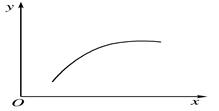
| x |
y |
|
| A |
温度 |
混合气体的平均相对分子质量 |
| B |
压强 |
A的百分含量 |
| C |
再通入A |
B的转化率 |
| D |
加入催化剂 |
A的质量分数 |
某温度下在容积为2 L的密闭容器中,发生2X(g)+Y(g)  2W(g)的反应,当充入1 mol X和1 mol Y,经20 s达到平衡时生成了0.4 mol W。下列说法正确的是( )
2W(g)的反应,当充入1 mol X和1 mol Y,经20 s达到平衡时生成了0.4 mol W。下列说法正确的是( )
| A.若升高温度,W的体积分数减小,则该反应ΔH<0 |
| B.以Y的浓度变化表示的反应速率为0.01 mol/(L·s) |
| C.在其他条件不变的情况下,增加1 mol X,则X和Y的转化率均提高 |
| D.增大压强正反应速率增大,逆反应速率减小,则平衡向正反应方向移动 |
在密闭容器中,反应X2(g)+Y2(g)  2XY(g) ΔH<0,达到甲平衡。在仅改变某一条件后,达到乙平衡,对此过程的分析正确的是( )
2XY(g) ΔH<0,达到甲平衡。在仅改变某一条件后,达到乙平衡,对此过程的分析正确的是( )
| A.图Ⅰ是增大压强的变化情况 |
| B.图Ⅱ是一定是加入催化剂的变化情况 |
| C.图Ⅲ是增大压强或升高温度的变化情况 |
| D.图Ⅲ一定是升高温度的变化情况 |
反应N2(g)+3H2(g)  2NH3(g) ΔH<0,在某一时间段中反应速率与反应过程的曲线如下图所示,则NH3的百分含量最低的一段时间是( )
2NH3(g) ΔH<0,在某一时间段中反应速率与反应过程的曲线如下图所示,则NH3的百分含量最低的一段时间是( )
| A.t0~t1 | B.t2~t3 | C.t3~t4 | D.t5~t6 |
在一定温度下,反应A2(g)+B2(g) 2AB(g)达到平衡状态的标志是()
2AB(g)达到平衡状态的标志是()
| A.容器内总的压强不随时间变化 |
| B.容器内的总物质的量不随时间变化 |
| C.单位时间内生成2n mol AB的同时生成n mol B2 |
| D.容器内A2、B2、AB的物质的量之比是1∶1∶2时的状态 |