乙醇分子结构中各种化学键如下所示,关于乙醇在各种反应中断键的说明不正确的为
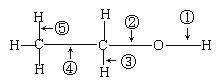
| A.和乙酸共热时,断裂①键 |
| B.和金属钠反应时,键①断裂 |
| C.和P2O5共热时,键②⑤断裂 |
| D.在铜催化下和氧气反应时,键①⑤断裂 |
下列化学用语表达正确的是
A.对硝基甲苯的结构简式: |
B.CH2F2的电子式: |
C.苯分子的比例模型: |
| D.16O2与18O2互为同素异形体 |
设NA为阿伏伽德罗常数的值。下列说法正确的是
A.5NH4NO3 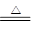 2HNO3+4N2↑+9H2O反应中,生成28 g N2,转移的电子数目为3.75NA 2HNO3+4N2↑+9H2O反应中,生成28 g N2,转移的电子数目为3.75NA |
| B.室温下,1 L pH=13的NaOH溶液中,由水电离的OH-数目为0.1NA |
| C.氢氧燃料电池正极消耗22.4 L(标准状况)气体时,电路中通过的电子数目为2NA |
| D.高温下,0.2 mol Fe与足量水蒸气反应,生成的H2分子数目为0.3 NA |
下列叙述正确的是
| A.将CO2通入BaCl2溶液中至饱和,无沉淀产生;再通入SO2产生沉淀 |
| B.在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉仍不溶解 |
| C.向AlCl3溶液中滴加氨水,产生白色沉淀;再加过量NaHSO4溶液,沉淀消失 |
| D.纯锌与稀硫酸反应产生氢气的速率较慢,再加入少量CuSO4固体,速率不变 |
下列行为中不符合促进“低碳经济”宗旨的是
| A.发展水电,开发新能源,如核能、太阳能、风能等,减少对矿物能源的依赖 |
| B.尽量使用含126C的产品,减少使用含136C或146C的产品 |
| C.推广煤的干馏、气化、液化技术,提供清洁、高效燃料和基础化工原料 |
| D.推广利用微生物发酵技术,将植物秸秆、动物粪便等制成沼气替代液化石油气 |
将0.6 mol A和0.5 mol B充入0.4 L密闭容器中发生2A(g)+B(g) mD(g)+E(g),经过5 min后达到化学平衡,此时测得D为0.2mol。又知5min内用E表示的平均反应速率为0.1 mol·L-1·min-1,下列结论正确的是
mD(g)+E(g),经过5 min后达到化学平衡,此时测得D为0.2mol。又知5min内用E表示的平均反应速率为0.1 mol·L-1·min-1,下列结论正确的是
A.A、B均转化了20%
B.m值为1
C.5 min内用A表示的平均反应速率为0.1 mol·L-1·min-1
D.平衡时混合物总物质的量为1 mol