下列做法存在安全隐患的是
①将水沿烧杯内壁缓缓加入浓硫酸中,用玻璃棒不断搅拌
②实验室制取氯气时,尾气用碱液吸收
③取用金属钠或钾做完实验后,剩余的药品要放回原瓶
④夜间厨房发生煤气泄漏时,应立即开灯检查煤气泄漏的原因,然后打开所有的门窗通风
⑤干冰可用于钠、镁等金属的灭火
| A.①④⑤ | B.①②③④ | C.①③④⑤ | D.全部 |
室温时,向10mL的醋酸稀溶液中逐滴滴入NaOH稀溶液至过量,有关叙述正确的是
| A.实验过程中水的电离程度的变化是先增大后减小 |
| B.当溶液呈中性时,反应恰好完全 |
| C.当反应恰好完全时,消耗NaOH溶液10mL |
| D.当溶液呈碱性时,其中离子浓度由大到小的顺序可能为c(Na+)>c(OH-)>c(Ac-)>c(H+) |
某化工厂的废水中含1%的H2SO4,采用边排放边处理成化肥硫铵的方法变废为宝(如图所示)。若处理后废水中的硫酸恰好全部转化为硫铵,则所用的20%氨水的流量为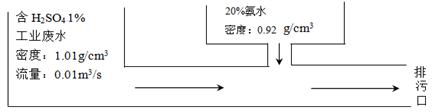
| A.1.98×10-3m3/s | B.5.49×10-4m3/s | C.1.90×10-4 m3/s | D.9.52×10-5 m3/s |
β-月桂烯的结构如图所示,一分子该物质与溴发生加成反应,得到的产物(只考虑位置异构)理论上最多有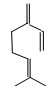
| A.6种 | B.7种 | C.8种 | D.9种 |
化学方程式是一种重要的化学用语。所写的化学方程式不能用来正确解释化学过程或事实的是
A.熔融烧碱时不能使用石英坩埚:SiO2 + 2NaOH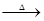 Na2SiO3 + H2O Na2SiO3 + H2O |
| B.在海带灰的浸出液(含有I-)中滴加H2O2得到I2: 2I- +3H2O2 + 2H+ → I2 + O2↑+ 4H2O |
| C.红热的铁丝与水接触,表面形成蓝黑色(或黑色)保护层: 3Fe + 4H2O(g) 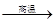 Fe3O4 + 4H2 Fe3O4 + 4H2 |
| D.“84消毒液”(有效成分NaClO)和“洁厕灵”(主要成分盐酸)混合使用时会放出氯气: |
ClO-+Cl-+2H+→ Cl2↑+H2O
25℃时,Kw =1.0×10-14;100℃时,Kw =5.4×10-13。对有关溶液pH说法正确的是
| A.100℃时,pH=12的NaOH(aq)和pH=2的H2SO4(aq)恰好中和,所得溶液的pH=7 |
| B.100℃时,0.2 mol/L Ba(OH)2(aq)和0.2 mol/L HCl(aq)等体积混合,所得溶液的pH=7 |
| C.25℃时,0.2 mol/L NaOH(aq)与0.2 mol/L CH3COOH(aq)恰好中和,所得溶液的pH="7" |
| D.25℃时,pH=12的氨水和pH=2的H2SO4(aq)等体积混合,所得溶液的pH>7 |