NaCl是一种化工原料,可以制备一系列物质(见图)。下列说法正确的是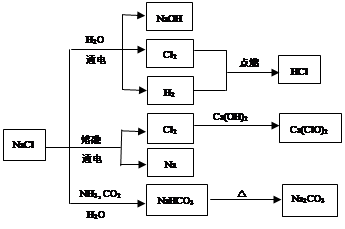
| A.25℃,NaHCO3在水中的溶解度比Na2CO3的大 |
| B.图中所示转化反应都是氧化还原反应 |
| C.常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应 |
| D.石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 |
据国外资料报道,在独居石(一种共生矿,化学成分为Ce、La、Nd等的磷酸盐)中,查明有尚未命名的116、124、126号元素.判断其中116号应位于周期表中的
| A.第六周期ⅣA族 | B.第七周期ⅥA族 |
| C.第七周期Ⅷ族 | D.第八周期ⅥA族 |
将一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如下。下列说法错误的是
| 物质 |
a |
b |
c |
d |
| 反应前质量/g |
6.40 |
3.20 |
4.00 |
0.50 |
| 反应后质量/g |
待测 |
2.56 |
7.20 |
0.50 |
| A.a和b是反应物,d可能是催化剂 |
| B.反应后a物质的质量为4.64g |
| C.c物质中元素的种类,一定和a、b二种物质中元素的种类相同 |
| D.若物质a与物质b的相对分子质量之比为2﹕1,则反应中a与b的化学计量数(系数)之比为2﹕l |
用NA表示阿伏加德罗常数,下列说法正确的是
| A.78g Na2O2与足量水反应中电子转移了2NA |
| B.只有在标准状况下NA个氧气分子的物质的量才是1mol |
| C.常温常压下,22.4L N2气体的分子数小于NA |
| D.20g D2O所含的中子数为9NA |
食品保鲜的措施有:添加防腐剂、充填保护气体、放置干燥剂和脱氧保鲜剂等。一次,小明在食用盒装月饼时,撕开了用于保鲜的小纸袋,发现其中盛放着一种灰黑色的粉末,几天后,看到灰黑色粉末变得有些发红。原保鲜剂粉末可能是





















| A.木炭粉 | B.铝粉 | C.还原性铁粉 | D.氧化铜粉末 |
生活中常会碰到的某些化学问题,如:①“白雪牌”漂粉精可令所有有色物质黯然失“色”,没有最白,只有更白;②霸王洗发液不含任何化学物质;③人喝了啤酒会打嗝,是因为啤酒中的碳酸盐与胃酸反应生成了二氧化碳;④53度白酒是指该白酒的着火点是53℃;⑤太太口服液含丰富的氮、磷、锌等微量元素。则有关上述说法,你的看法是
| A.全部正确 | B.只有①⑤正确 |
| C.只有③⑤正确 | D.以上说法都是错误的 |