在氨水中存在下列电离平衡:NH3·H2O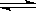 NH+OH-,下列情况能引起电离平衡向正向移动的有 ( )
NH+OH-,下列情况能引起电离平衡向正向移动的有 ( )
①加NH4Cl固体 ②加NaOH溶液 ③加HCl
④加CH3COOH溶液 ⑤加水 ⑥加热煮沸
| A.①③⑤ | B.①④⑥ | C.③④⑤ | D.①②④ |
酸雨主要是燃烧含硫燃料所放出的SO2造成的,现取500mL雨水样,每隔一定时间测试其pH,数据如下: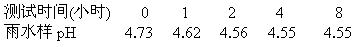
则雨水样的pH放置时减小的原因是
| A.SO2仍源源不断溶解而达饱和 | B.雨水样中的某物质发生氧化 |
| C.水缓慢蒸发溶液渐渐浓至饱和 | D.又有SO2少量溶于雨水样里 |
选用一种试剂就可以一次把物质的量浓度相同的Na2SO4、Na2SO3、Na2CO3、Na2S、BaCl2五种无色溶液加以区别,这种试剂是
| A.CaCl2 | B.Ba(OH)2 | C.H2SO4 | D.HCI |
下列离子能在同一无色溶液大量共存的是
| A.Na+、Cu2+、Cl―、SO42― |
| B.K+、HCO3―、Cl―、OH― |
| C.K+、Na+、Cl―、Ag+ |
| D.Na+、K+、SO42-、OH― |
判断溶液为中性的依据是
| A.c(OH-)=1×10-7 mol/L | B.c(H+)=1×10-7 mol/L | C.c(OH-)=c(H+) | D.pH=7 |
下列电离方程式正确的是
A. |
B.CH3COOH→CH3COO-+H+ |
C. |
D.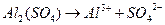 |