某溶液仅含Fe2+、Na+、Mg2+、Ba2+、SO42-、NO3-、Cl-中的4种离子,所含离子的物质的量均为1mol。若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。下列说法不正确的是 ( )
| A.该溶液中所含的离子是:Fe2+、Na+、SO42-、NO3- |
| B.若向该溶液中加入过量的稀硫酸和KSCN溶液,溶液显血红色 |
| C.若向该溶液中加入过量的稀硫酸,产生的气体遇空气能变成红棕色 |
| D.若向该溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为72g |
在0.1 mol/L的醋酸钠溶液中加入等体积的下列物质,溶液中离子浓度大小关系正确的是( )
| A.水;c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
| B.0.1 mol/L盐酸;c(Na+)=c(Cl-)>c(H+)>c(CH3COO-)>c(OH-) |
| C.0.1 mol/L醋酸;c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D.0.1 mol/L氢氧化钠;c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
在蒸发皿中用酒精灯加热蒸干下列物质的溶液然后灼烧,可以得到该物质固体的是( )
| A.AlCl3 | B.Na2SO3 | C.KMnO4 | D.MgSO4 |
下列离子方程式中,属于水解反应的是( )
A.HCOOH+H2O HCOO-+H3O+ HCOO-+H3O+ |
B.CO2+H2O HCO3-+H+ HCO3-+H+ |
C.CO32-+H2O HCO3-+OH- HCO3-+OH- |
D.HS-+H2O S2-+H3O+ S2-+H3O+ |
如图表示某物质发生的是( )
已知水的电离平衡曲线如图所示,试回答下列问题: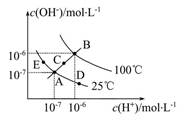
(1)图中五点Kw间的关系是。
(2)若从A点到D点,可采用的措施是。
a.升温b.加入少量的盐酸 c.加入少量的NH4Cl
(3)E对应的温度下,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为。