中学化学教材中有大量数据,下列是某同学对数据利用情况,正确的是( )
| A.利用焓变的数据或熵变的数据一定都能单独判断反应是否能自发进行 |
| B.利用反应热数据的大小判断不同反应的反应速率的大小 |
| C.利用沸点数据推测将一些液体混合物分离开来的可能性 |
| D.利用溶液的pH与7的大小关系,判断PH=6.8的溶液一定显酸性 |
下列有关说法中正确的是(不考虑立体异构)( )
| A.丁烷与戊烷分子内碳原子数相差一个,但同分异构体数却相差两个 |
| B.有机物CH3(CH2)2CH(CH3)2的一氯代物有5种 |
| C.汽油、煤油、植物油均为含碳、氢、氧三种元素的化合物 |
| D.0.1 mol分子式为C4H4O的有机物完全燃烧,消耗氧气的体积为11.2 L(标准状况下) |
某有机物的结构简式为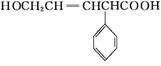 ,该有机物不可能发生的化学反应是( )
,该有机物不可能发生的化学反应是( )
| A.加成反应 | B.酯化反应 | C.氧化反应 | D.水解反应 |
分子式为C5H12O的醇与C5H10O2的酸发生酯化反应最多可形成酯( )
| A.8种 | B.16种 | C.24种 | D.32种 |
下列涉及的有机物及有机反应类型的说法中正确的是( )
| A.乙烯分子与苯分子中碳碳键不同,但二者都能发生加成反应 |
| B.除去甲烷中的乙烯可以将混合气体通过盛有足量NaOH溶液的洗气瓶 |
| C.苯的二氯代物有3种,说明苯分子是由6个碳原子以单双键交替结合而成的六元环结构 |
| D.乙酸与乙醇在浓硫酸作用下可以反应,该反应属于加成反应 |
下列关于有机物的说法中错误的是( )
| A.CCl4可由CH4制得,可萃取碘水中的碘 |
| B.淀粉、油脂、蛋白质都能水解,但水解产物不同 |
| C.乙醇、乙酸、乙酸乙酯都能发生取代反应,乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去 |
| D.苯不能使KMnO4溶液褪色,因此苯不能发生氧化反应 |