(6分)实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。进行此实验,所用仪器如下图:
(1)连接上述仪器的正确顺序是(填各接口处的字母): 接 ,_____接 ,________接 , 接 。
(2)在装置中:①饱和食盐水起的作用是 ,浓硫酸起的作用是 。
有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色黏稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
(1)称取A 9.0 g,升温使其汽化,测其密度是相同条件下H2的45倍。
实验结论:A的相对分子质量为。
(2)将此9.0 g A在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4 g和13.2 g。则A的分子式为。
(3)另取A 9.0 g,跟足量的NaHCO3粉末反应,生成2.24 L CO2(标准状况),若与足量金属钠反应则生成2.24 L H2(标准状况)。
实验结论:A中含有的官能团:、________。
(4)A的核磁共振氢谱如图: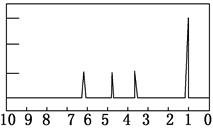
实验结论:A中含有种氢原子。
(5)综上所述,A的结构简式_________________。
有相对分子质量为58的几种有机物,试写出符合条件的有机物的结构简式:
(1)若该有机物为烃,则可能的结构简式为:、。
(2)若该有机物是一种饱和一元醛,则其结构简式为:。
(3)若该有机物1mol能与足量银氨溶液作用可析出4molAg,则其结构简式为:。写出该物质的氧化产物与还原产物反应生成高聚酯的化学方程式。
(4)若该有机物能与金属钠反应,又能使溴的四氯化碳溶液褪色,则该有机物可能是:。(注羟基连在双键碳上的有机物极不稳定)
某物质只含C、H、O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键)。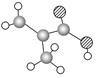
(1)该物质的结构简式为。
(2)该物质中所含官能团的名称为。
(3)下列物质中,与该产品互为同系物的是,与该产品互为同分异构体的是。(填序号)
①CH3CH="==CHCOOH"
②CH2===CHCOOCH3
③CH3CH2CH===CHCOOH
④CH3CH(CH3)COOH
合成氨对化学工业和国防工业有重要意义。若向合成塔中按物质的量之比l:4充入N2、H2进行氨的合成,图A为T℃时平衡混合物中氨气的体积分数与压强(p)关系图。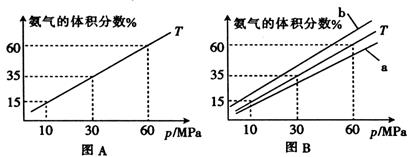
(1)图A中压强为10 MPA时,N2的转化率为
(2)已知:在合成氨反应中,升高温度H2的转化率降低。
①若图B中T=450℃,则温度为500℃时对应的曲线是(填“A”或“B”)
②该反应达到平衡时某物理量随温度变化如下图所示,纵坐标可以表示的物理量有
| A.H2的逆反应速率 |
| B.N2的质量百分含量 |
| C.NH3的的体积分数 |
| D.混合气体的平均相对分子质量 |
通常用燃烧的方法测定有机物的分子式,可在燃烧室内将有机物样品与纯氧在电炉加热下充分燃烧,根据产品的的质量确定有机物的组成。下图所示的是用燃烧法确定有机物分子式的常用装置。 现准确称取一定量某烃样品,经燃烧后A管增重2.2 g, B管增重1.08g。请回答:
现准确称取一定量某烃样品,经燃烧后A管增重2.2 g, B管增重1.08g。请回答:
(1)按上述所给的测量信息,装置的连接顺序应是:D
(2)C管中浓硫酸的作用是
(3)该有机物在纯氧中充分燃烧的化学方程式为(有机物用分子式表示)
(4)若该有机物分子中含有4个甲基,则该有机物的结构简式为