对于反应2SO2+O2 2SO3,下列判断正确的是
2SO3,下列判断正确的是
| A.2体积SO2和足量O2反应,必定生成2体积SO3 |
| B.其他条件不变,增大压强,平衡必定向右移动 |
| C.平衡时SO2消耗速度必定等于O2生成的速度 |
| D.平衡时SO2浓度必定等于O2浓度的两倍 |
NaCl是海水中提取出来的一种重要物质,除食用外,它还是一种工业原料,下列以NaCl为原料的产品(或物质)是
①烧碱 ②纯碱 ③金属钠 ④氯气 ⑤盐酸
| A.①②③④⑤ | B.①②③④ | C.①②③⑤ | D.①②④⑤ |
相同质量的C6H6、C7H8、C4H10、C3H6完全燃烧时,耗氧量最多的是
| A.C6H6 | B.C7H8 | C.C4H10 | D.C3H6 |
X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示,若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是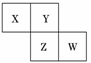
| A.最高价氧化物对应水化物的酸性W比Z弱 |
| B.只由这四种元素不能组成有机化合物 |
| C.Z的单质与氢气反应较Y剧烈 |
| D.X、Y形成的化合物都易溶于水 |
下列有机物中有两种氢原子且其氢原子数之比为3:2的化合物是
A. |
B.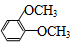 |
C.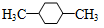 |
D.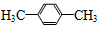 |
一定温度下,在一容积不变的密闭容器中发生的可逆反应2X(g)  Y(g)+Z (s),以下能说明作为反应达到平衡标志的是
Y(g)+Z (s),以下能说明作为反应达到平衡标志的是
| A.X的分解速率与Y的消耗速率相等 |
| B.X、Y与Z的物质的量之比为2:1:1 |
| C.混合气体的密度不再变化 |
| D.单位时间内生成lmolY的同时分解2mol X |