KNO3和KCl在不同温度时的溶解度如下表所示。
| 温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
|
| 溶解度/g |
KNO3 |
13.3 |
20.9 |
31.6 |
45.8 |
63.9 |
85.5 |
110 |
138 |
| KCl |
27.6 |
31.0 |
34.0 |
37.0 |
40.0 |
42.6 |
45.5 |
48.3 |
请回答下列问题:
(1)20℃时,KNO3的溶解度是 。
(2)30℃时,将KNO3和KCl固体各40g分别加入两只盛有100g水的烧杯中,能得到饱和溶液的是 。将上述得到的不饱和溶液转化为该温度下的饱和溶液,可采用的一种方法是 。
(3)依据上表中数据,已绘制出KNO3和KCl的溶解度曲线(如右图所示),图中能表示KNO3溶解度曲线的是 (填“m”或“n”)。 
(4)从含有少量KCl的KNO3饱和溶液中得到较多的KNO3晶体,通常可采用的方法是 。
(5)由表中数据分析可知,KNO3和KCl在某一温度t时具有相同的溶解度,则t的取值范围是 。
如图是A、B、C三种固体物质的溶解度曲线,请回答:
(1)曲线中P点表示 .
(2)t2℃时将相同质量的A、B、C三种物质分别加入到100g水中,充分溶解后,只有一种固体物质完全溶解了,这种物质是 .
(3)t2℃时,A、B、C三种物质的饱和溶液同时降温到t1℃,此时三溶液中溶质质量分数的大小关系是 .
请根据下表回答有关问题(各小题均用序号表示)
| 序号 |
① |
② |
③ |
④ |
| 物质 |
醋酸 |
水 |
熟石灰 |
小苏打 |
| 化学式 |
CH3COOH |
H2O |
Ca(OH)2 |
|
(1)请在表格中的横线上补充小苏打的化学式.
(2)表中的物质属于氧化物的是 .(用序号表示)
(3)若要测定醋酸溶液的酸碱度,可选用下列选项中的 .(用序号表示)
①无色酚酞试液②紫色石蕊试液③pH试纸.
如图为同学们使用的一种碳素墨水笔,在组成这种墨水笔的各种材料中:
(1)属于有机高分子材料的是 ;(选填一种即可,下同)
(2)写出其中的一种金属材料与硫酸铜溶液发生反应的化学方程式: 。 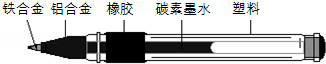
某农田作物生长需要3.5kg氮元素,若施用尿素来提供这些氮元素,则需要尿素 kg
用化学用语填空:
(1)2个碳原子 ;
(2)n个过氧化氢分子 ;
(2)3个铝离子 ;
(4)高锰酸钾中锰元素显+7价 .