将铁的化合物溶于盐酸,滴加KSCN溶液不发生颜色变化,再加入适量氯水,溶液立即呈红色的是 ( )
| A.Fe2O3 | B.FeCl3 | C.Fe3O4 | D.FeO |
若某原子的摩尔质量是Mg·mol-1,则一个该原子的真实质量是
下列条件下,两瓶气体所含原子数一定相等的是
①同质量、不同密度的N2和CO;②同温度、同体积的N2和H2;
③同体积、同密度的C2H4和C3H6;④同压强、同体积的N2O和CO2
| A.①② | B.②③ |
C.③④ | D.①③ |
下列仪器使用前必须检查其是否漏水的是
①分液漏斗②蒸馏烧瓶③冷凝管④容量瓶⑤蒸发皿⑥长颈漏斗
| A.②⑥ | B.①④ | C.③④ | D.③⑤ |
研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到的直观形象的效果。下列表达错误的是
A.密闭容器中CuO和C高温反应的气体产物: 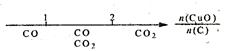 |
B.Fe在Cl2中的燃烧产物: 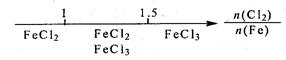 |
C.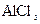 溶液中滴加NaOH后铝的存在形式: 溶液中滴加NaOH后铝的存在形式: 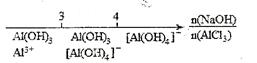 |
D.氨水与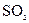 反应后溶液中的铵盐: 反应后溶液中的铵盐: |

国际无机化学命名委员会将长式元素周期表原先的主、副族号取消,从左往右改为18列,碱金属为第 1列,稀有气体为18列。按这个规定,下列说法错误的是
1列,稀有气体为18列。按这个规定,下列说法错误的是
| A.只有第2列元素的原子最外层有2个电子 |
| B.第3~12列中的元素都是金属元素 |
| C.室温时,第18列元素的单质都是气体 |
| D.第16、17列元素都是主族元素 |