已知
(l)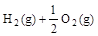 =H2O(g) △H1=a kJ·
=H2O(g) △H1=a kJ·
(2)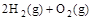 =2H2O(g) △H2=b kJ·
=2H2O(g) △H2=b kJ·
(3)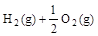 =H2O(l) △H3=c kJ·
=H2O(l) △H3=c kJ·
(4)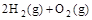 =2H2O(l) △H4=d kJ·
=2H2O(l) △H4=d kJ·
下列关系式中正确的是( )
| A.a<c <0 | B.b>d>0 | C.2a=b<0 | D.2c=d>0 |
关于氢键,下列说法不正确的是
| A.每一个水分子内含有两个氢键 |
B.冰、水中 都存在氢键 都存在氢键 |
| C.水是一种非常稳定的化合物,这由于水分子之间形成氢键无关 |
| D.水的沸点很高,原因之一是水分子间存在氢键 |
下列叙述正确的是
| A.NaHSO4、Na2O2晶体中的阴、阳离子个数比均为1∶2 |
| B.离子化合物中一定不含共价键 |
| C.某主族元素的最高价含氧酸为HnROm,则其气态氢化物一般是H8-2m+nR或RH8-2m+n |
| D.元素周期表中L层电子为奇数的元素的化合价也都是奇数 |
已知1-18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同电子层结构,下列关系正确的是
| A.质子数:c>b | B.离子的还原性:Y2->Z- |
| C.氢化物的稳定性:H2Y>HZ | D.原子半径:X<W |
一些科学家预言,存在稳定的超重元素,如Z=114,N=184的原子,下列说法中正确的是
| A.第七周期可能有50种元素 | B.该原子的质量数为184 |
| C.该元素位于第七周期第ⅣB族 | D.该原子核外有114个电子 |
分别处于第二、三周期的主族元素A和B,它们离子的电子层相差两层,已知A处于第m族,B处于第n族,A只有正化合价,则A、B原子核外的电子总数分别为
A.m+2、10+n B.m、n
C.3、7 D.m-2、10-n