氯酸钾和二氧化锰共热制取氧气,已知反应前混合物共15.5g,反应完全后剩余固体10.7g,问分解出氧气多少克?剩余固体混合物中二氧化锰多少克?(友情提示:化学方程式为2KClO3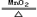 2 KCl + 3O2↑)
2 KCl + 3O2↑)
甲、乙、丙三位同学分别取铁粉和铜粉的均匀混合物与某稀硫酸反应,所得数据如下:
计算:
(1)金属混合物铁的质量分数;
(2)甲制得硫酸亚铁的质量;
(3)该稀硫酸的质量分数。
2008年9月,中国爆发三鹿婴幼儿奶粉受污染事件,导致了食用受污染奶粉的婴幼儿产生肾结石病症,其原因是奶粉中含有三聚氰胺,三聚氰胺的分子式为C3H6N6。请计算:
(1)三聚氰胺的相对分子质量;
(2)三聚氰胺中C、H、N三种元素的质量比;
(3)已知婴幼儿奶粉中蛋白质的国家标准含量为150g/kg,现在发现某种奶粉中每千克含三聚氰胺2.563g。假设,奶粉中只有蛋白质和三聚氰胺两种化合物含氮元素。问,如果通过含氮量检测,要达到150g/kg蛋白质含量标准,每千克奶粉中至少要掺入
克蛋白质才可以达到要求?(蛋白质(由各种氨基酸构成,不确定)中含氮量约为30%)
为测定某样品中锌的质量分数,取10g此样品,分五次向其中加入稀硫酸使之充分反应(假设锌的样品中杂质不与稀硫酸反应,且不溶于水),每次加入的稀硫酸质量及测定剩余固体的质量,记录数据如下表:
| 第一次 |
第二次 |
第三次 |
第四次 |
第五次 |
|
| 加入稀硫酸的质量/g |
10 |
10 |
10 |
10 |
10 |
| 剩余固体质量/g |
8.4 |
6.8 |
5.2 |
3.6 |
3.6 |
请认真分析表中的数据,回答下列问题:
(1)表示样品与稀硫酸恰好完全反应的是上表中第________次操作;
(2)计算样品中锌的质量分数;
(3)计算实验中所用稀硫酸的溶质质量分数。
人体缺乏维生素C(简写“Vc”)就会患坏血病。右图为某种“维生素C”的说明书的一部分,试分析问答:
| 维生素C(白色) 化学式:C6H8O6 每片100mg含Vc 不少于10% 一日三次,每次 xx片,饭后服用 |
⑴“Vc”的相对分子质量是;
“Vc”中碳、氢、氧元素的质量比是。
⑵若正常成年人每天最低需要补充“Vc”60mg。
①当“Vc”完全由图中“维生素C”来补充时,则每次至少服用片;
②当“Vc”完全由某种蔬菜(每100g这种蔬菜含“Vc”15mg) 来补充时,则每天至少应该食用这种蔬菜g。
取某碳酸钠样品放入烧杯中,加入95.8g水充分溶解,再向其中加入稀硫酸,反应放出气体的总质量与所加入稀硫酸的质量关系曲线如下图所示,请根据题意解答问题: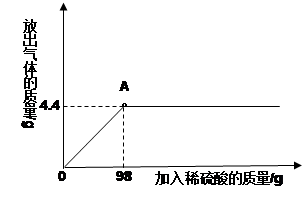
(1)当加入196g稀硫酸时,
放出气体的质量为g。
(2)计算加入的稀硫酸溶液溶质
的质量分数为 。
(3)试通过计算求出加入98g稀硫酸
(即A点)时烧杯中溶液溶质的质量分数。
(写出计算过程)