在以下化学反应中,能证明次氯酸是一种弱酸的是( )
| A.Cl2+H2O=HCI+HClO |
B.2HClO 2HCl+O2↑ 2HCl+O2↑ |
| C.Ca(ClO)2+HCl=CaCl2+2HClO |
| D.Ca(ClO)2+CO2+H2O=CaCO3+2HClO |
若醋酸用HAc表示,则在0.1mol·L-1 NaAc溶液中,下列离子浓度关系正确的是
| A.c(Na+)= c(Ac—)+c(HAc) |
| B.c(Na+)+c(OH—)= c(Ac— )+c(H+) |
| C.c(Na+)>c(OH—) > c(Ac—) > c(H+) |
| D.c(Na+)> c(Ac—)> c(H+)> c(OH—) |
设nA是阿伏加德罗常数的数值。下列说法正确的是
| A.1L 0.1mol·L-1的FeCl3溶液中,Fe3+的数目为0.1nA |
| B.1molNH3中含有N-H键的数目为3nA |
| C.7.8g Na2O2中含有的阳离子数目为0.1nA |
| D.标准状况下,22.4L水中分子个数为nA |
下列表述中,合理的是
| A.将水加热,Kw增大,pH不变 |
| B.NaHCO3溶液中存在6种分子或离子 |
| C.用25 mL碱式滴定管量取20.00mL高锰酸钾溶液 |
| D.用惰性电极电解足量的AgNO3溶液时,当有0.2 mole-转移时会析出21.6g银 |
右图为一原电池的结构示意图,下列说法中,错误的是 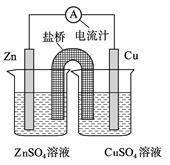
| A.Cu电极为正电极 |
| B.原电池工作时,电子从Zn电极流出 |
| C.原电池工作时的总反应为:Zn+Cu2+=Zn2++Cu |
| D.盐桥(琼脂-饱和KCl溶液)中的K+移向ZnSO4溶液 |
一定量的稀盐酸跟过量锌粉反应时,为了减缓反应速率又不影响生成H2的总量,可采取的措施是
| A.加入少量稀NaOH溶液 | B.加入少量CH3COONa固体 |
| C.加入少量NH4HSO4固体 | D.加入少量Na2CO3浓溶液 |