某元素原子的核电荷数为9,其原子核内的质子数为 ,该元素原子的一价阴离子中,质子数 ,核外电子数为 。
下图中X是无支链的、具有果香味的合成香料,可用于调配多种果香型香精。已知D在标准状况下的密度为1.25 g/L,其产量可以用来衡量一个国家石油化工发展水平。E是生活中常见的一种有机物。各物质间转化关系如下: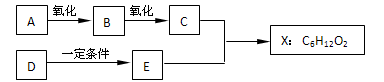
请回答下列问题。
(1)A分子的名称是。
(2)B分子中所含官能团是。
(3)C+E→X的化学反应类型是反应。
(4)写出任意两种与A具有相同官能团的A的同分异构体的结构简式(不含A):
、。
(5)X与氢氧化钠溶液反应的化学方程式。
以D为原料生产一种常见塑料的化学方程式是。
某有机物A的相对分子质量为62。为进一步测定A 的化学式,现取6.2 g A完全燃烧,得到二氧化碳和水蒸气。将产物先后通过足量的浓硫酸和碱石灰,两者分别增重5.4 g和8.8 g(假设每步反应完全)。
(1)该有机物的实验式是 ________________;分子式是 ______________。
(2)红外光谱显示有“C—C”键和“O—H”键的振动吸收,若核磁共振氢谱只有2个吸收峰且峰面积之比为1∶2,推断该有机物的结构简式是 _______________________。
(3)该有机物与金属钠反应的化学方程式是______________________________________。
短周期主族元素A、B、C、D、E、的原子序数依次增大,A和B形成5个原子核的分子,A和C形成3个原子核的分子,且两种分子均含有10个电子。D的原子半径最大,A、B、D、E与C形成的化合物均有两种,其中E与C形成的化合物中的一种能使品红溶液褪色。
则由A、B、C三种元素组成的中学常见的化合物中:
①甲燃烧则其耗氧量与乙烯相同则甲的结构简式是。
②若乙能发生银镜反应则乙的化学式或结构简式是。
③若丙分子中的B、A、C最简个数比为1:2: 1且丙能与D发生反应,则丙的结构简式
④若丁标况下蒸汽密度为3.93g/L,B%=54.5%,A%=9.1%,且丁能发生水解反应则丁的结构简式为。
⑤若戊在同条件下密度为H2的22倍,4.4g该物质完全燃烧产物依次通过浓硫酸增重3.6g,碱石灰增重8.8g则戊的结构简式为。
下图为原电池的示意图。请回答: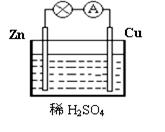
(1)Zn极为原电池的(填“正”或“负”)极,该极的电极反应式是,属于(填“氧化反应”或“还原反应”)。
(2)(填“电子”或“电流”)从锌片通过导线流向铜片,溶液中的H+从(填“锌片”或“铜片”)获得电子
写出下列反应的方程式 (1)乙烯可使溴的四氯化碳溶液褪色,该反应方程式为,
(1)乙烯可使溴的四氯化碳溶液褪色,该反应方程式为,
(2)苯与液溴在催化剂条件下反应的化学方程式为。
(3)写出苯与氢气反应反应方程式