下列叙述正确的是( )
| A.NaOH 溶液能导电,所以 NaOH 溶液是电解质 |
| B.固体KCl 不导电,但KCl 是电解质 |
| C.氯化氢的水溶液能导电,所以HCl 是电解质 |
| D.CO2的水溶液能导电,所以CO2是电解质 |
如图所示是元素周期表的一部分,X、Y、Z、W均为短周期元素,若w原子最外层电子数是其内层电子数的7/10,则下列说法中不正确的是
| A.原子半径由大到小排列顺序Z>Y>X |
| B.Y元素的两种同素异形体在常温下都是气体 |
| C.最高价氧化物对应水化物的酸性Z>W |
| D.阴离子半径由大到小排列顺序X>Y>Z>W |
两种微粒的质子数和电子数均分别相等,它们不可能是
| A.一种阳离子和一种阴离子 | B.一种单质和一种化合物分子 |
| C.一种分子和一种离子 | D.一种原子和一种分子 |
下列分子含有的电子数目与HF相同,且只有两个极性共价键的是
| A.CO2 | B.H2O | C.N2O | D.CH4 |
将纯锌片和纯铜片按图示 方式插入同浓度的稀硫酸中一段时间,叙述正确的是
方式插入同浓度的稀硫酸中一段时间,叙述正确的是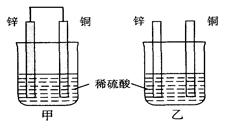
| A.两烧杯中铜片表面均无气泡产生 |
| B.甲中铜片是正极,乙中铜片是负极 |
| C.甲中铜被氧化,乙中锌被氧化 |
| D.产生气泡的速率甲比乙快 |
反应E+F=G在温度t1下进行 ,反应M+N=K在温度t2下进行,已知t1>t2,且E和F的浓度均大于M和N的浓度(其他条件均相同),则两者
,反应M+N=K在温度t2下进行,已知t1>t2,且E和F的浓度均大于M和N的浓度(其他条件均相同),则两者 的反应速率
的反应速率
| A.前者大 | B.后者大 | C.相等 | D.无法判断 |