根据热化学方程式:S(s) + O2(g)= SO2(g) △H =" -297.23" kJ·mol-1,下列说法正确的是:
| A.1 mol SO2 (g)的能量总和大于1 mo S(s)和1 mol O2(g)的能量总和 |
| B.1 mol SO2(g)的能量总和小于1 mol S(s)和1 mol O2(g)的能量总和 |
| C.S(g) + O2(g) = SO2(g)△H =" -Q" kJ·mol-1;Q的值大于297.23 |
| D.S(g) + O2(g)= SO2(g)△H =" -Q" kJ·mol-1;Q的值等于297.23 |
X、Y、Z是三种常见的单质,甲、乙是两种常见的化合物。下表各组物质之间通过一步反应不能实现如图所示转化的是()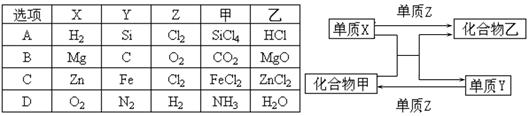
下列装置或操作不能达到实验目的的是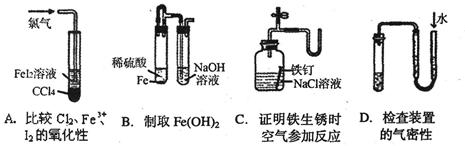
用NA表示阿伏加德罗常数的值。下列叙述正确的是()
| A.3.6 g碳与3.36 L O2一定条件下恰好完全反应,生成CO分子数一定为0.3NA |
| B.6.9 g钠与足量的CO2和H2O (g)混合气体充分反应,转移的电子数一定为0.3NA |
| C.25℃时, 0.15mol/L的Na2CO3溶液中,Na+数目为0.3NA |
| D.标准状况下,2.24L氯仿中含有C-Cl数目为0.3NA |
下列化学用语表示正确的是()
A.NaH与重水反应的方程式:NaH+D2O=NaOH+D2↑ |
B.三氟化氮的电子式: |
| C.熔融状态下硫酸氢钠的电离方程式:NaHSO4(熔融)=Na++HSO4- | |
D.质量数为137的钡原子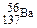 |
在25℃时,用石墨电极电解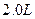 ,
,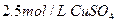 溶液。5min后,在一个石墨电极上有6.4g Cu生成。试回答:
溶液。5min后,在一个石墨电极上有6.4g Cu生成。试回答:
(1)转移电子的物质的量,得到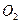 的体积(标准状况),溶液的
的体积(标准状况),溶液的 ?
?
2)如用等质量的两块铜片代替石墨作电极,电解后两铜片的质量相差多少?电解液的 是否变化?(相对原子质量 Cu:64)
是否变化?(相对原子质量 Cu:64)