科学家预测原子序数为114的元素,具有相当稳定性的同位素,它的位置在第7周期IVA族,称为类铅。关于它的性质,预测错误的是
| A.它的最外层电子数为4 | B.它的金属性比铅强 |
| C.它具有+2、+3、+4价 | D.它的最高价氧化物的水化物是强酸 |
通过溶解、过滤、蒸发等操作,可将下列各组混合物分离的是
| A.硝酸钠氢氧化钠 | B.氧化铜二氧化锰 |
| C.氯化钾碳酸钙 | D.硫酸铜氢氧化钠 |
下列物质中属于强电解质的是
| A.NH3 | B.乙醇 | C.Cu | D.NaCl |
化学与社会、生产、生活密切相关。下列说法正确的是
| A.加快化石燃料的开采和使用 |
| B.NaHCO3可用于治疗胃酸过多 |
| C.明矾可用于水的杀菌消毒 |
| D.从海水中提取物质都必须通过化学反应才能实现 |
在如图所示装置中进行氨的催化氧化实验:往三颈瓶内的浓氨水中不断通入空气,将红热的铂丝插入瓶中并接近液面。反应过程中,可观察到瓶中有红棕色气体产生,铂丝始终保持红热。下列有关说法错误的是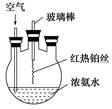
A.反应后溶液中含有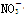 |
| B.实验过程中NH3·H2O的电离常数不可能发生变化 |
| C.实验过程中有化合反应发生 |
| D.反应后溶液中c(H+)增大 |
已知常温下AgCl的Ksp=1.8×10-10,AgI的Ksp=8.5×10-17。若在常温下,向5mL含有KCl和KI各为0.01mol/L的溶液中加入8 mL 0.01 mol/L AgNO3溶液,此时溶液中所含溶质的离子浓度大小关系正确的是
| A.c(K+)>c(NO3-)>c(Ag+)=c(Cl-)+c(I-) |
| B.c(K+)>c(NO3-)>c(Ag+)>c(Cl-)>c(I-) |
| C.c(NO3-)>c(K+)>c(Ag+)>c(Cl-)>c(I-) |
| D.c(K+)>c(NO3-)>c(Cl-)>c(Ag+)>c(I-) |