某地有甲、乙两工厂排放污水,污水中各含有下列8种离子中的4种(两厂不含相同的离子):Ag+、Ba2+、Fe3+、Na+、SO42-、NO3-、OH-、Cl-。两厂单独排放都会造成严重的水污染,如将两厂的污水按一定比例混合,沉淀后污水便变成无色澄清的只含硝酸钠而排放,污染程度大大降低。关于污染源的分析,你认为正确的是
| A.SO42-和NO3-可能来自同一工厂 |
| B.Cl-和NO3-一定在不同的厂 |
| C.Ag+和Na+可能来自同一工厂 |
| D.Na+和NO3-一定不来自同一工厂 |
下列过程一定释放出能量的是
| A.化合反应 | B.分解反应 | C.分子拆成原子 | D.原子结合成分子 |
对于溶液的酸碱性说法正确的是()
| A.c(H+)很小的溶液一定呈碱性 | B.pH等于7的溶液一定呈中性 |
| C.c(H+)=c(OH-)的溶液一定呈中性 | D.不能使酚酞试液变红的溶液一定呈酸性 |
向0.1 mol·L-1的CH3COOH溶液中加入CH3COONa晶体或加水稀释时,均会引起()
| A.溶液的pH都增加 | B.CH3COOH电离程度增大 |
| C.溶液导电能力都减弱 | D.溶液中c(OH-) 都减小 |
能表示人喝水时的胃液的pH变化的图像是()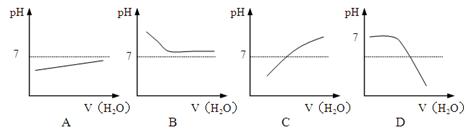
用某种仪器量一液体体积时,平视读数为V1mL,仰视读数为V2mL,俯视读数为V3mL,若V2>V1>V3,则所使用仪器可能是
| A.容量瓶 | B.量筒 |
| C.碱式滴定管 | D.以上仪器均不可 |