据《中国环境报》报道,某化工厂排放的污水,使某市一条长约50公里的河水受到严重污染,对工农业生产及人民的生活造成严重危害。经环保部门测定,被污染的河水pH在1~4之间,其他水质指标也严重超标。2002年6月1日,国家环境保护总局发布的《地表水环境质量标准》,对地表水质量作了明确规定,部分指标如下(除pH外,各项目的单位: mg/L):
| 水质分类 项目及标准 |
I类 |
II类 |
III类 |
IV类 |
V类 |
| 磷(P)≤ |
0.02 |
0.1 |
0.2 |
0.3 |
0.4 |
| 氮(N)≤ |
0.2 |
0.5 |
1.0 |
1.5 |
2.0 |
| 锌(Zn)≤ |
0.05 |
1.0 |
1.0 |
2.0 |
2.0 |
| 铅(Pb)≤ |
0.01 |
0.01 |
0.05 |
0.05 |
0.1 |
| pH |
6~9 |
6~9 |
6~9 |
6~9 |
6~9 |
(1).如让你测定河水样的酸碱度,可选用
A.石蕊试液 B.酚酞试液 C.pH试纸 D.碳酸钠溶液
(2)材料2中所指出的 “氮”、“磷”、“锌”、“铅”,是指A.单质 B.元素 C,离子 D.分子
(3)经测定,该化工厂排放的污水中铅的质量分数为(1X10-5)%。则该污水的水质
属于(设该污水的密度为1g/cm3) A.I类 B.Ⅲ类 C.Ⅳ类 D.V类
可逆反应:N2(g)+3H2(g) 2NH3(g)的正逆反应速率可用反应物或生成物的浓度变化来表示,下列各关系中能说明反应已达平衡状态的是()
2NH3(g)的正逆反应速率可用反应物或生成物的浓度变化来表示,下列各关系中能说明反应已达平衡状态的是()
| A.3V(N2)正=V(H2)正 | B.V(N2)正=V(NH3)逆 |
| C.2V(H2)正=3V(NH3)逆 | D.V(N2)正=3V(H2)逆 |
在一定温度下的定容密闭容器中,当反应A2(g)+B2(g) 2AB(g)达到平衡的标志()
2AB(g)达到平衡的标志()
| A.单位时间内生成nmolA2的同时也生成nmolAB |
| B.容器内的压强不随时间变化而变化 |
| C.单位时间内生成nmolA2的同时也生成nmolB2 |
| D.单位时间内生成2nmolAB的同时也生成nmolB2 |
在一定条件下,可逆反应:mA+nB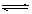 pC达到平衡,若:
pC达到平衡,若:
(1)A、C是气体,增加B的量,平衡不移动,则B为态。
(2)A、C是气体,而且m+n=p,增大压强可使平衡发生移动,则平衡移动的方向是。
(3)加热后,可使C的质量增加,则正反应是反应(放热或吸热)。
在已经处于化学平衡状态的体系中,如果下列量发生变化,其中一定能表明化学平衡移动的是()
| A.反应混合物的浓度 | B.反应体系的压强 |
| C.正、逆反应的速率 | D.反应物的转化率 |
设C+CO2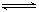 2CO-Q1(吸热反应)反应速率为 u1,N2+3H2
2CO-Q1(吸热反应)反应速率为 u1,N2+3H2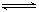 2NH3+Q2(放热反应)反应速率为 u2,对于上述反应,当温度升高时,u1和u2的变化情况为()
2NH3+Q2(放热反应)反应速率为 u2,对于上述反应,当温度升高时,u1和u2的变化情况为()
| A.同时增大 | B.同时减小 | C.增大,减小 | D.减小,增大 |