在我国居民平衡膳食宝塔(每人每日摄入量) 中人体三大营养物质糖类主要来源于 , 蛋白质主要来源于 ,油脂主要来源于 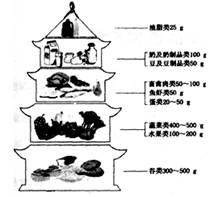
糖尿病是影响人们身体健康的一种常见病,临床表现为尿糖含量高,控制尿糖,是控制病情的常用途径。检验病情时,将尿糖检测试纸浸入热的鲜尿中,取出后,观察试纸颜色变红的程度,并与标准色卡进行比较,以确定尿糖的浓度,据此回答:
(1)尿糖试纸是将滤纸剪成小条,在一种浊液中浸润一段时间,再在一定条件下干燥而成。对该方法而言,这种浊液中的有效成分是,该成份中决定其化学性质的原子团名称为,该物质能发生的反应有(填序号)①与活泼金属钠反应,②一定条件下与醋酸反应,③碱性条件下发生消去反应,④使灼热的黑色氧化铜变红,⑤一定条件下与氢气反应。
(2)这种方法用来检测尿糖的原理是,其化学反应方程式为。
某校化学兴趣小组的同学按图所示将实验装置连接好,进行化学能与热能转化的实验探究。请帮他们回答下列问题: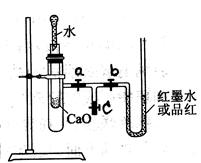
实验前,在U型管内加入少量品红溶液(或红墨水)。打开3个T型管螺旋夹,使U型管内两边的液面处于同一水平面,再夹紧螺旋夹。
(1)在内部的试管里盛1g氧化钙,当滴入2mL左右的蒸馏水后,打开a、b螺旋夹,可观察到U型管里的红墨水如何变化?____________________________________________________。
(2)如果用这个装置观察到U型管内出现与上述(1)相反的现象,可在小试管中加入________固体后滴入适量的蒸馏水。
(3)若向内部的试管中放入几小块铜片,再用滴管滴入10mL稀硝酸,能否得到(1)中现象?,另外可观察到的现象是;产生上述现象的原因是;写出有关反应的化学方程式;由此可知,反应后产物的总能量(填“大于”、“小于”、“等于”)硝酸和铜片的总能量。此时该装置有明显的不足,原因是,改进的方法是。
随着人类社会活动的加剧,我们地球人已面临能源危机,能高效地利用现有能源和开发新能源已受到各国的高度重视。试回答下列问题:
(1)为提高燃料利用率,可通过改进汽油组成的办法来改善汽油的燃烧性能。例如,“无铅汽油”是在汽油中加入CH3OC(CH3)3得到的,在CH3OC(CH3)3分子中必然存在的原子间连接形式有(填写编号)。①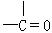 ,②
,②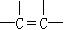 ,③
,③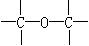 ,④
,④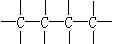 。
。
(2)天然气燃烧的产物无毒、热值高,而且管道输送方便,是值得推广的一种清洁能源,已成为我国西部开发的重点项目之一。天然气的主要成分是,它的空间结构是,下列说法中能证明它是该结构的理由是(填写编号)。
①其一氯取代物不存在同分异构体,②其二氯取代物不存在同分异构体,③它是非极性分子。
(3)为解决能源危机,有效开发民用氢能源是一条卓有实效的途径,为制得廉价的氢气,下列制氢方法中可行的途径是(填写编号)。①电解水②锌和稀硫酸反应③光解海水
根据所学知识回答下列问题,在如图所示装置中 ,
,
(1)若烧杯中溶液为稀硫酸,则观察到的现象为,正极反应式为,负极反应式为,
该装置中的能量变化形式为。
(2)若烧杯中溶液为氢氧化钠溶液,则负极为,装置中总反应方程式为。
X、Y、Z为三种短周期元素,他们在周期表中的位置关系如图所示 。据此回答下列问题:
。据此回答下列问题:
(1)X元素的名称为,它形成的单质为(用分子式表示); He。若该元素的某种原子内核内中子数与质子数相等,则该原子的摩尔质量是;结合最近卫星发回的图片预测,月球的土壤中吸附着数百万吨的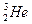 ,上述原子与
,上述原子与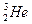 的关系是。
的关系是。
(2)Y元素形成单质的电子式是,Y单质的氧化性(填“强于”或者“弱于”)O2的氧化性,并用相应的化学方程式说明。
(3)元素Z在自然界中的存在形态为(填序号)①只有化合态,②只有游离态,③既有游离态,又有化合态;含Z元素的某些化合物燃烧后会造成严重的大气污染,其主要原因是。
(4)Y元素、Z元素与H2化合时的能量变化是,(填“都放热”、“都吸热”、“前者放热,后者吸热”或者“前者吸热,后者放热”),能量变化的大小关系为前者(填“>”、“=”或者“<”)。