镭是元素周期表中第七周期的ⅡA族元素。下面关于镭的性质的描述中不正确的是( )
| A.在化合物中呈+2价 | B.单质使水分解、放出氢气 |
| C.氢氧化物呈两性 | D.碳酸盐难溶于水 |
下列说法中正确的是
| A.0.1mol/L (NH4)2SO4溶液中:c(SO42—) > c(NH4+) > c(H+) > c(OH-) |
| B.pH=4的醋酸稀释l0倍,溶液中c(CH3COOH)、c(OH﹣)均减小 |
| C.常温下向CH3COONa溶液中加入适量CH3COOH溶液,使混合液的pH=7,则混合液中c(Na+)=c(CH3COO—) |
| D.等浓度的弱酸HA溶液和NaOH溶液等体积混合,所得混合液显碱性 |
有关下图的说法正确的是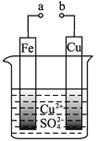
| A.构成原电池时Cu极反应为: Cu﹣2e-=Cu2+ |
| B.构成原电池时溶液中SO42- 移向Cu极 |
| C.要使Fe极不被腐蚀,Cu片换Zn片或a接直流电源负极 |
| D.形成电解池,Cu电极不可能溶解 |
下列说法正确的是
| A.氨的催化氧化是一种特殊的固氮方式 |
| B.工业冶炼铝:电解熔融AlCl3固体 |
| C.将铁粉加入FeCl3、CuCl2混合溶液中,充分反应后剩余的固体中不一定有铁 |
| D.用加热分解的方法可将NH4Cl固体和Ca(OH)2固体的混合物分离 |
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示。其中Y所处的周期序数与族序数相等。下列说法正确的是
| X |
|||
| Y |
Z |
W |
A.原子半径:Y<Z<W
B.气态氢化物的稳定性:X>Z
C.W的最高价氧化物与水反应形成的化合物是离子化合物
D.X的气态氢化物的水溶液能与Y的最高价氧化物对应水化物发生反应
设nA为阿伏伽德罗常数的数值,下列说法正确的是
| A.常温常压下,8gO2含有2nA个电子 |
| B.10L 0.1mol·L-1的氨水中有nA个NH4+ |
| C.标准状况下,22.4L盐酸含有nA个HCl分子 |
| D.1molNa与足量氧气反应生成Na2O和Na2O2的混合物,失去nA个电子 |