下列叙述正确的是 ( )
| A.1 mol H2O的质量为18g/mol |
| B.3.01×1023个SO2分子的质量为32g |
| C.CH4的摩尔质量为16g |
| D.标准状况下,1 mol任何物质体积均为22.4L |
已知合成氨的反应为:N2 + 3H2  2NH3 ΔH=" -" 92.4 KJ/mol在一定条件下达到化学平衡,现升高温度使平衡发生移动,下列图像中能正确描述正、逆反应速率(v)变化的是
2NH3 ΔH=" -" 92.4 KJ/mol在一定条件下达到化学平衡,现升高温度使平衡发生移动,下列图像中能正确描述正、逆反应速率(v)变化的是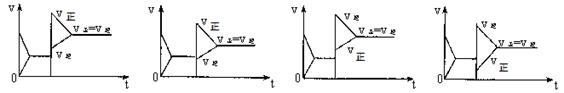
A BCD
对于密闭容器中进行的反应CO(g)+H2O(g) CO2 (g) +H2 (g),达到平衡后,其他条件不变,增大CO的浓度,下列说法不正确的是
CO2 (g) +H2 (g),达到平衡后,其他条件不变,增大CO的浓度,下列说法不正确的是
| A.正反应速率增大 |
| B.逆反应速率先减小 |
| C.达到平衡时,逆反应速率比原平衡要大 |
| D.化学平衡常数不变 |
只改变一个影响因素,平衡常数K与化学平衡移动的关系叙述错误的是
| A.K值不变,平衡可能移动 | B.K值变化,平衡一定移动 |
| C.平衡移动,K值可能不变 | D.平衡移动,K值一定变化 |
一定条件下反应 2AB(g) A2(g)+B2(g)达到平衡状态的标志是
A2(g)+B2(g)达到平衡状态的标志是
A.容器中混合气体的质量不随时间变化
B.容器内三种气体 AB、A2、B2共存
C.v正(AB)=2v逆(A2)
D.单位时间内消耗n mol A2,同时生成2n mol AB
某硫酸铝溶液密度为1.28g·cm-3,其中铝离子的质量分数为5.3%,200mL该溶液中SO42-离子的物质的量约等于
| A.0.21mol | B.0.35mol | C.0.5mol | D.0. 75mol |