密度为0.91 g·cm-3的氨水,质量分数为25%,若将此氨水用等体积的水稀释后,所得溶液的质量分数为 ( )
| A.大于12.5% | B.小于12.5% |
| C.等于12.5% | D.无法确定 |
25℃时进行四组实验,其中“实验内容”与对应“现象或结论”关系错误的是
| 选项 |
实验内容 |
现象或结论 |
| A |
向2SO2+O2 2SO3的平衡体系中加入由18O构成的氧气 2SO3的平衡体系中加入由18O构成的氧气 |
则SO2中的18O的含量会增加 |
| B |
向pH=1的盐酸和醋酸各0.5L的溶液中各加入1.4g铁粉 |
醋酸中生成H2的速率快且最终气体量多 |
| C |
以石墨为电极,电解KI溶液(其中含有少量酚酞和淀粉) |
阴极逸出气体且附近溶液渐呈红色 |
| D |
以Pb为负极,硫酸溶液为电解质的铅蓄电池,在放电过程中 |
负极质量增加,SO42-向负极迁移,溶液pH增大 |
下列离子方程式书写正确的是
| A.向KI与稀硫酸的混合溶液中通入氧气:4H++O2+6I- = 3I2+2H2O |
| B.亚硫酸钠溶液与双氧水混合:SO32-+2H2O2 = SO42-+2H2O+O2↑ |
| C.a mol FeI2溶液中通入2a mol Cl2:2Fe2++4I-+3Cl2 = 2I2+2Fe3++6C1- |
| D.硅酸钠溶液中通入过量的CO2:SiO32-+CO2+H2O = H2SiO3↓+CO32- |
设NA表示阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,1.12L1H2和0.1g 2H2均含有0.1NA个质子 |
| B.在同压不同温的情况下,质量相同的氧气和臭氧所含氧原子数不相同 |
| C.标准状况下,11.2L庚烷完全燃烧后生成的CO2分子数为3.5NA |
| D.常温下,将5.6 g 铁投入足量的浓硫酸中转移电子数为0.3 NA |
将三种黑色粉末组成的混和物加入到足量的某热浓酸中,充分反应后得到蓝绿色溶液和两种气体。将从蓝绿色溶液中分离得到的盐与0.15mol还原铁粉恰好反应完全,可得浅绿色溶液和6.4g红色沉淀;将上述生成的两种气体通入足量饱和NaHCO3溶液中,仍然收集到两种气体,据此推断黑色粉末可能为
| A.物质的量 FeS:CuO:Fe =1:1:1 | B.物质的量 C:CuO:Fe =3:2:2 |
| C.质量 MnO2:CuO:C=5.5:8:12 | D.质量 Fe:C:CuO=7:5:3 |
对于实验Ⅰ~Ⅳ的描述正确的是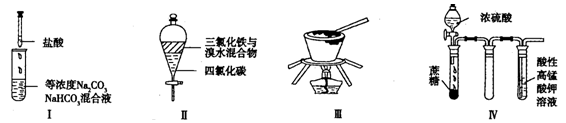
| A.实验Ⅰ:逐滴滴加稀盐酸时,试管中立即产生大量气泡 |
| B.实验Ⅱ:充分振荡后静置,下层溶液为橙红色,上层无色 |
| C.实验Ⅲ:从饱和食盐水中提取氯化钠晶体 |
| D.装置Ⅳ:酸性KMnO4溶液中有气泡出现,且溶液颜色逐渐变浅乃至褪去 |