用黄色的FeCl3溶液分别进行下列实验,解释或结论不正确的是
| |
实验 |
现象 |
解释或结论 |
| A |
加入FeCl3固体 |
溶液变成红褐色 |
FeCl3的水解程度变大 |
| B |
加入等体积水 |
溶液颜色变浅 |
c(Fe3+)变小 |
| C |
加入足量Fe粉 |
溶液颜色变浅绿色 |
2Fe3++ Fe=3Fe2+ |
| D |
将FeCl3溶液微热 |
溶液变成红褐色 |
水解反应ΔH>0 |
检验某未知溶液是否含有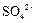 ,下列操作最合理的是()
,下列操作最合理的是()
| A.加入HNO3酸化的Ba(NO3)2溶液 |
| B.加入盐酸酸化的BaCl2溶液 |
| C.先用盐酸酸化,若有沉淀产生,过滤,在滤液中再加BaCl2溶液 |
| D.先加BaCl2溶液,若有沉淀产生,再加盐酸 |
下列反应中,调节反应物用量或浓度,不会改变反应产物的是()
| A.铁在硫蒸气中燃烧 | B.H2S在空气中燃烧 |
| C.二氧化硫通入澄清石灰水 | D.硫酸中加入锌粉 |
下列有关浓H2SO4性质的叙述中,错误的是()
| A.浓硫酸具有脱水性,因而能使蔗糖炭化 |
B.在反应HCOOH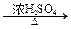 CO↑+H2O中,浓H2SO4只表现脱水性 CO↑+H2O中,浓H2SO4只表现脱水性 |
C.在反应Cu+2H2SO4(浓)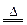 CuSO4+SO2↑+2H2O中,浓H2SO4只表现氧化性 CuSO4+SO2↑+2H2O中,浓H2SO4只表现氧化性 |
| D.浓硫酸具有吸水性,因而能使CuSO4·5H2O转化为CuSO4 |
下列说法正确的是()
| A.ⅠA族元素的金属性一定比ⅡA族元素的金属性强 |
| B.ⅥA族元素的氢化物中,稳定性最好的其沸点也最高 |
| C.同主族元素单质的熔沸点从上到下逐渐升高 |
| D.第三周期元素的离子半径,从左到右逐渐减小 |
在F、P、S三种元素中,每种元素都有某些方面区别于其他两种元素;若从中选出氟元素,选择的理由是()
| A.单质与冷水反应非常剧烈 | B.单质固态时属于分子晶体 |
| C.一定条件下,能与氢气发生化合反应 | D.最高价氧化物对应的水化物是强酸 |