某温度下,在一个2L的密闭容器中,加入4molA和2molB进行如下反应: 3A(s)+2B(g)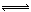 4C(g)+D(g),反应2min后达到平衡,测得生成l.6molC,下列说法正确的是
4C(g)+D(g),反应2min后达到平衡,测得生成l.6molC,下列说法正确的是
| A.前2min,D的平均反应速率为0.2mol·L-1·min-1。 |
| B.此时,B的平衡转化率是40% |
| C.增大该体系的压强,平衡不移动,化学平衡常数不变 |
| D.增加B,平衡向右移动,B的平衡转化率增大 |
酸根RO3-所含电子数比硝酸根NO3-的电子数多10。则下列说法正确的是
| A.R原子的电子层数比N的电子层数多2 |
| B.R元素的最高正化合价与NO3-中的N的化合价相等 |
| C.R所含电子数比N的电子数多10 |
| D.R和N为同族元素 |
下列方程式正确的是
| A.铁和稀硝酸反应:Fe + 2H+ = H 2↑+ Fe 2+ |
| B.向氯化铵的溶液中加入足量浓NaOH溶液并加热:NH4++OH-△NH3↑+H2O |
| C.Ba(OH)2溶液与H2SO4溶液混合产生沉淀:Ba2++ SO42-=BaSO4↓ |
| D.往NaOH溶液通入过量SO2: SO2+2OH-="=" SO32-+H2O |
下列除杂的操作方法,正确的是
| A.NH3中混有少量水蒸气:通过装有浓硫酸的洗气瓶 |
| B.CO2中混有少量SO2气体:通入NaOH溶液 |
| C.食盐固体中混有少量NH4Cl:加热 |
| D.硝酸混有少量硫酸:加适量BaCl2溶液后再过滤 |
X、Y、Z是3种短周期元素,其中X、Y位于同一主族,Y、Z处于同一周期。X原子的最外层电子数是次外层电子数的3倍。Z原子的核外电子数比Y原子少1。下列说法正确的是
A元素非金属性由强到弱的顺序是: Z> Y>X
B.Y元素最高价氧化物对应水化物的化学式可表示为H4YO4
C.3种元素的气态氢化物中,Z的气态氢化物最稳定
D.原子半径由大到小的顺序为 Z >Y>X
下列事实不能用来说明Cl非金属性比S强的是
| A.气态HCl比H2S稳定 | B.HCl酸性比H2SO3强 |
| C.还原性:S2-比Cl-强 | D.Cl2通入NaBr溶液中生成Br2 |