下列叙述正确的是( )
| A.SO2的水溶液能够导电,但SO2是非电解质 |
| B.饱和氯水的导电性很好,所以氯气是强电解质 |
C. 和 和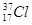 为不同的核素,二者核外电子数不同 为不同的核素,二者核外电子数不同 |
| D.化合反应和分解反应一定属于氧化还原反应 |
下列有关甲苯的实验事实中,能说明侧链对苯环性质有影响的是
| A.甲苯与浓硝酸反应生成三硝基甲苯 | B.甲苯能使酸性高锰酸钾溶液褪色 |
| C.甲苯燃烧产生带浓烟的火焰 | D.1 mol甲苯与3 mol H2发生加成反应 |
由1,3—丁二烯合成2—氯—1,3—丁二烯的路线如下:
该路线中各步的反应类型分别为
| A.加成、水解、加成、消去 | B.取代、水解、取代、消去 |
| C.加成、取代、取代、消去 | D.取代、取代、加成、氧化 |
酯A水解后可生成酸X和醇Y,若Y被氧化后可得到酸X,则A不可能是
下列物质的任意比例混合,若总物质的量一定,则充分燃烧消耗氧气及生成水的量均相等的是
| A.C2H6 , C2H6O | B.C3H6 , C4H6O2 |
| C.C2H2 , C2H4O | D.C3H6O , C4H8O2 |
下列有机物中,所有原子可能处于同一平面的是
| A.乙烷 | B.甲苯 | C.丙炔 | D.苯乙烯 |