室温下,将 4 mol A 气体和 2 mol B 气体在 2 L 的密闭容器中混合并在一定条件下发生如下反应:2A(气)+B(气)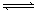 XC(气),经 2 s(秒)后反应达平衡,测得 C 的浓度为 0.6 mol·L-1 ,B的物质的量为1.4 mol,现有下列几种说法:
XC(气),经 2 s(秒)后反应达平衡,测得 C 的浓度为 0.6 mol·L-1 ,B的物质的量为1.4 mol,现有下列几种说法:
①用物质 A 表示的反应的平均速率为 0.3 mol·L-1·s-1
②反应前容器内的压强与平衡后容器内的压强之比为1:1
③ 2 s 时物质A的转化率为30%
④ X="2"
⑤室温下该反应的化学反应平衡常数是0.5
⑥其他条件不变,向容器中再加入1 molC气体,达到新平衡时,C的体积分数不变
其中正确的是( )
| A.①③④ | B.①④⑥ | C.②③⑤ | D.③⑤⑥ |
下列可以说明乙酸是弱酸的事实是
| A.乙酸不能使酚酞溶液变红色 | B.乙酸能使紫色石蕊试液变红色 |
| C.乙酸和Na2CO3反应可放出CO2 | D.0.1mol/L的乙酸溶液pH>1 |
在一只25 mL的碱式滴定管中注入0.1 mol/L的氢氧化钠溶液,其液面恰好在5mL的刻度处,若把滴定管中的溶液全部放入烧杯中,则所得溶液的体积
| A.大于20mL | B.小于20mL | C.等于20mL | D.等于5mL |
将NO3-+ Zn +OH-+H2O → NH3 +Zn(OH)42-配平后,离子方程式中OH-的化学计量数是
| A.1 | B.3 | C.5 | D.7 |
下列分子中,所有原子均在同一平面上的是
| A.CH3CH2CH2CH3 | B.CH3CH==CHCH3 |
| C.CH2==CHC≡CH | D.HC≡CCH3 |
下列各组离子一定能大量共存的是
| A.含有大量Fe3+的溶液中:NH4+、Na+、CI-、SCN- |
| B.在强碱溶液中:Na+、K+、AlO2-、CO32- |
| C.在c(H+)=10-13mol·L-1的溶液中:NH4+、Al3+、SO42-、NO3- |
| D.在pH=1的溶液中:K+、Fe2+、Cl-、NO3- |