下列反应常温时能自发进行,并既能用能量判据又能用熵判据解释的是( )
| A.HCl(g)+NH3(g)=NH4Cl(s) |
| B.2KClO3(s)=2KCl(s)+3O2(g) |
| C.2Na2O2(s)+2H2O(l)=4NaOH(s)+O2(g) |
| D.Ba(OH)2·8H2O(s)+2NH4Cl(s)=BaCl2(s)+ 2NH3(g)+10H2O(l) |
托盘天平两盘内分别放入一个质量相同的烧杯,烧杯里有200 mL 1.00 mol·L-1的盐酸,天平平衡。向烧杯中分别加入下列各组中的两种金属(每个烧杯只放其中一种金属),反应结束后,天平仍保持平衡的是( )。
| A.8 g Mg和8 g Al |
| B.1 g Mg和1 g Al |
| C.0.1 mol Mg和0.1 mol Al |
D.1.8 g Mg和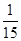 mol Al mol Al |
向含I-和Cl-的稀溶液中滴入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示。则原溶液中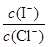 的比值为( )。
的比值为( )。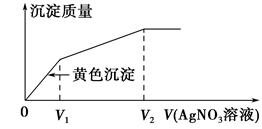
| A.(V2-V1)/V1 | B.V1/V2 | C.V1/(V2-V1) | D.V2/V1 |
碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种粒子之间的转化关系如图所示。下列说法中不正确的是( )。
| A.用淀粉—KI试纸和食醋检验加碘盐时淀粉—KI试纸会变蓝 |
| B.足量Cl2能使湿润的、已变蓝的淀粉—KI试纸退色的原因可能是5Cl2+I2+6H2O=2HIO3+10HCl |
| C.由图可知氧化性的强弱顺序为Cl2>I2>IO3- |
| D.途径Ⅱ中若生成1 mol I2,则反应中转移的电子数为10NA |
某无色溶液中可能含有I-、NH4+、Cu2+、SO32-,向该溶液中加入少量溴水,溶液呈无色,则下列关于溶液组成的判断正确的是( )。
①肯定不含I-;②肯定不含Cu2+;③肯定含有SO32-;④可能含有I-
| A.①③ | B.①②③ | C.①③④ | D.②③④ |
粗碘中通常含ICl和IBr,称为卤素互化物,其性质和卤素单质相似,都是较强的氧化剂,而且受热时ICl和IBr皆可像I2一样升华,在粗碘中加入以下选项中的一种物质后,再进行升华可制得精碘,应加入的物质是( )。
| A.H2O | B.Zn | C.KI | D.KCl |