市场上销售的“84”消毒液,其商品标示上注明:①本品为无色液体呈碱性 ②使用时应加水稀释 ③可对餐具、衣物进行消毒,可漂白浅色衣物。其可能的有效成分是
| A.Cl2 | B.SO2 | C.NaClO | D.KMnO4 |
草木灰中含有碳酸钾,它属于( )。
| A.氮肥 | B.钾肥 | C.复合肥料 | D.微量元素肥料 |
下列化学肥料均属于复合肥料的是( )。
| A.KH2PO4和NH4Cl | B.NH4Cl和NH4NO3 |
| C.KNO3和KH2PO4 | D.NH4Cl和KNO3 |
北京奥运会期间对大量盆栽鲜花施用了S诱抗素制剂,以保持鲜花盛开。S诱抗素的分子结构如图,下列关于该分子说法正确的是( )。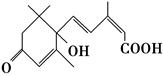
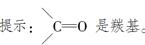
| A.含有碳碳双键、羟基、羰基、羧基 |
| B.含有苯环、羟基、羰基、羧基 |
| C.含有羟基、羰基、羧基、酯基 |
| D.含有碳碳双键、苯环、羟基、羰基 |
水可以造福人类,但水被污染后却给人类造成了灾难,为了防止水污染,下面①~⑤的措施中可以采用的是( )。
①禁止使用农药和化肥
②不任意排放工业废水
③抑制水中植物的生长
④生活污水经过净化处理再排放
⑤减少空气中硫的氧化物和氮的氧化物的含量
| A.②③④ | B.②④⑤ | C.①④⑤ | D.①②④ |
搞好兴奋剂管理是确保2008年奥运会成功举办的主要措施之一。国家体育总局转发了世界兴奋剂机构《2008年禁用清单》,违禁药物有216种,甲异炔诺酮(tibolone)是其中之一,它的结构简式如下,下列有关说法不正确的是( )。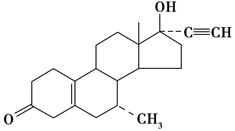
| A.甲异炔诺酮中含有的官能团有羟基、碳碳三键、碳碳双键及羰基 |
| B.甲异炔诺酮分子中含有4个手性碳原子 |
| C.1 mol甲异炔诺酮在浓硫酸作用下脱去1分子水,所得产物有两种 |
| D.1 mol甲异炔诺酮与足量的氢气催化加成,最多消耗4 mol H2 |